Soutenance de la thèse de Laurine Nieuwjaer Ziane – 26 Septembre 2023
Laurine Nieuwjaer Ziane soutiendra sa thèse intitulée « Développement d'un dispositif d'illumination pour le traitement de la carcinose péritonéale d'origine ovarienne par thérapie [...]
Publication de la norme NF G20-030 : Textiles lumineux - Détermination de l'éclairement énergétique et de la luminance d'étoffes lumineuses
La norme NF G20-030 : Textiles lumineux - Détermination de l'éclairement énergétique et de la luminance d'étoffes lumineuses vient d’être publiée. OncoThAI, en particulier, Elise [...]
Une fabrication facile de micro-aiguilles solubles contenant de l'acide 5-aminolévulinique
L'article intitulé "Une fabrication facile de micro-aiguilles solubles contenant de l'acide 5-aminolévulinique" de Mathilde CHAMPEAU et collaborateurs est désormais en ligne. Ce projet est [...]
Le projet PRODYNOV s’inscrit dans une thématique d’étude visant au développement des stratégies de photodiagnostic et de thérapie photodynamique des lésions péritonéales. L’objectif de notre équipe multidisciplinaire est de réunir les conditions nécessaires au développement d’un traitement photodynamique applicable en clinique humaine pour le traitement des carcinoses péritonéales d’origine ovarienne.
Cette démarche impose l’amélioration des techniques de modélisation de la cavité péritonéale, le développement de procédés d’illumination adaptés à ses contraintes, et l’utilisation de photosensibilisateurs de nouvelle génération ciblant les lésions de carcinose avec une meilleure spécificité pour améliorer la tolérance du traitement.
Contexte et enjeux
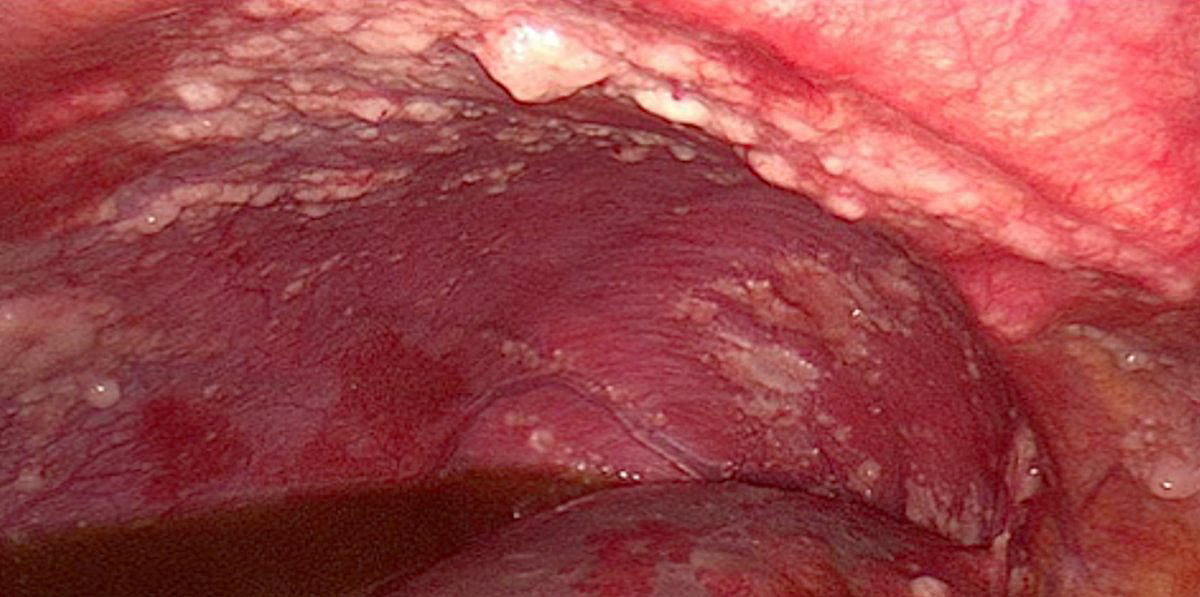
Le cancer de l’ovaire concerne 4 500 nouveaux cas chaque année en France. Le mauvais pronostic de la maladie est lié au retard diagnostic puisque la majorité des cas sont diagnostiqués aux stades III et IV de la Fédération Internationale de Gynécologie Obstétrique (FIGO). Ces stades sont marqués par l’existence de métastases péritonéales dont le traitement représente un enjeu pour le chirurgien car le taux de récidive locale est élevé et directement lié à la qualité de l’exérèse chirurgicale.
La prise en charge actuelle associe lorsqu’elle est possible, une chirurgie à une chimiothérapie reposant sur l’utilisation de sels de platine. Certaines thérapies ciblées sont venues récemment compléter cet arsenal thérapeutique. Il est admis que l’absence de lésions résiduelles après la chirurgie est le facteur principal de bon pronostic. La capacité du traitement chirurgical à éradiquer l’ensemble des implants tumoraux est donc décisive.
L’existence de lésions péritonéales microscopiques et la fréquence des récidives péritonéales imposent le développement de stratégies complémentaires.
La thérapie photodynamique est une option intéressante car elle est adaptée au traitement de surface étendue. Elle peut être associée à un photodiagnostic et une chirurgie guidée par la fluorescence.
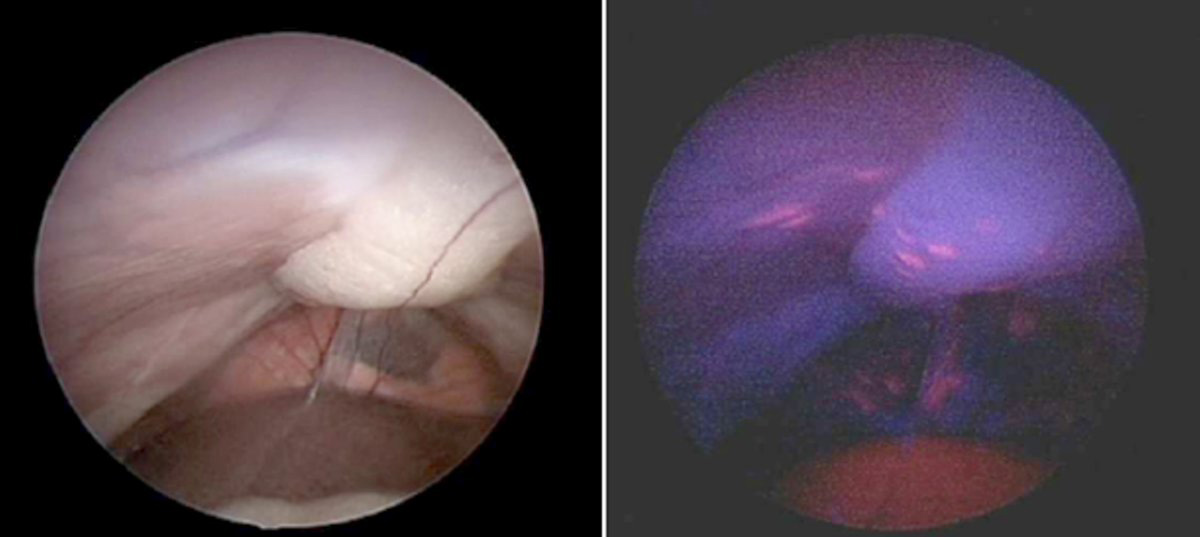
Nous souhaitons développer une technique alternative déjà appliquée dans d’autres disciplines, en proposant le photodiagnostic et la thérapie photodynamique des lésions de carcinose péritonéale ovarienne. Nous sommes convaincus que la réalisation d’une séance de thérapie photodynamique en complément d’une chirurgie de cytoréduction complète permettrait la destruction des lésions microscopiques et la diminution du taux de récidive péritonéale.
Thérapie photodynamique
La thérapie photodynamique (PDT) est une stratégie alternative qui présente plusieurs avantages : traitement de surface, ciblage spécifique des cellules tumorales, possibilité d’être associée à d’autres traitements, faible coût potentiel. La réaction photodynamique repose sur l’activation d’un photosensibilisateur par une lumière de longueur d’onde spécifique qui conduit, en présence d’oxygène, à la production d’espèces réactives de l’oxygène cytotoxiques.
Il a ainsi été montré par notre équipe qu’il était possible d’induire efficacement une nécrose des microlésions péritonéales par la mise en œuvre d’un protocole de PDT sur lignée cellulaire in vitro et sur un modèle animal in vivo.

De nombreux facteurs peuvent influer sur la sécurité et les résultats de la PDT : choix du photosensibilisateur et spécificité de ce dernier pour le tissu cible, puissance totale délivrée et vitesse d’administration (irradiance), longueur d’onde d’excitation, intervalle entre l’injection du PS et l’application de la lumière. Le traitement de l’ensemble de la cavité abdominale nécessite aussi la mise au point d’une nouvelle procédure d’illumination. De récents travaux de notre équipe sur modèle animal ont pu montrer que des illuminateurs souples permettaient d’assurer une illumination homogène.
Dans le cadre de travaux collaboratifs, des textiles lumineux de grandes dimensions, parfaitement adaptés à l’illumination de la cavité péritonéale, ont pu être conçus.

Perspectives
La fréquence des récidives péritonéales après traitement fait discuter les limites de la chirurgie de cytoréduction, qui ne permettra pas le contrôle de la maladie microscopique, et la problématique des chimiorésistances.
En offrant la possibilité de traiter localement des lésions disséminées sur une large surface, la PDT apparaît théoriquement comme un candidat pertinent pour le traitement des carcinoses péritonéales d’origine ovarienne.
Le cancer de l’ovaire doit être considéré comme un ensemble de sous-groupes de maladies distinctes. La PDT doit répondre à cette exigence scientifique de personnalisation des traitements. L’essor des thérapies ciblées et la découverte de cibles moléculaires spécifiques, à l’image du récepteur au folate, peuvent contribuer à envisager une application clinique de la PDT intrapéritonéale. Un photosensibilisateur plus spécifique devrait en effet permettre d’améliorer la tolérance de la procédure, de limiter le nombre des complications, et ainsi de donner une place à la PDT intrapéritonéale dans l’arsenal thérapeutique disponible aujourd’hui. L’équipe du Laboratoire Réactions et Génie des Procédés (UMR 7274 CNRS - Université de Lorraine, Nancy, France) apporte son expertise pour le design et la synthèse de photosensibilisateurs adaptés.

Nous étudions par ailleurs en collaboration avec l’équipe CNRS UMR 8161 (Institut de Biologie de Lille, France) les spécificités de la réponse immune anticancéreuse après PDT. Cet aspect du traitement est un axe de recherche à part entière dans la mesure où associé à la toxicité directe liée au traitement, il pourrait exister un effet abscopal contribuant à conférer un rôle protecteur au traitement. Il a été démontré que la PDT pouvait modifier le sécrétome des cellules tumorales entraînant l’activation du métabolisme mitochondrial des cellules immunitaires.
Plusieurs paramètres sont impliqués pour la mise en œuvre du traitement (photosensibilisateurs, source lumineuse, dosimétrie, biologie). Il est donc essentiel d’avoir une réflexion globale pour développer ces différentes composantes afin de proposer un protocole efficace, simple et reproductible pour les cliniciens. Notre équipe multidisciplinaire réunit ces différents acteurs et dispose des conditions requises pour atteindre cet objectif.
Besoin de plus d'informations sur Prodynov ? Contactez-nous
Contexte et enjeux
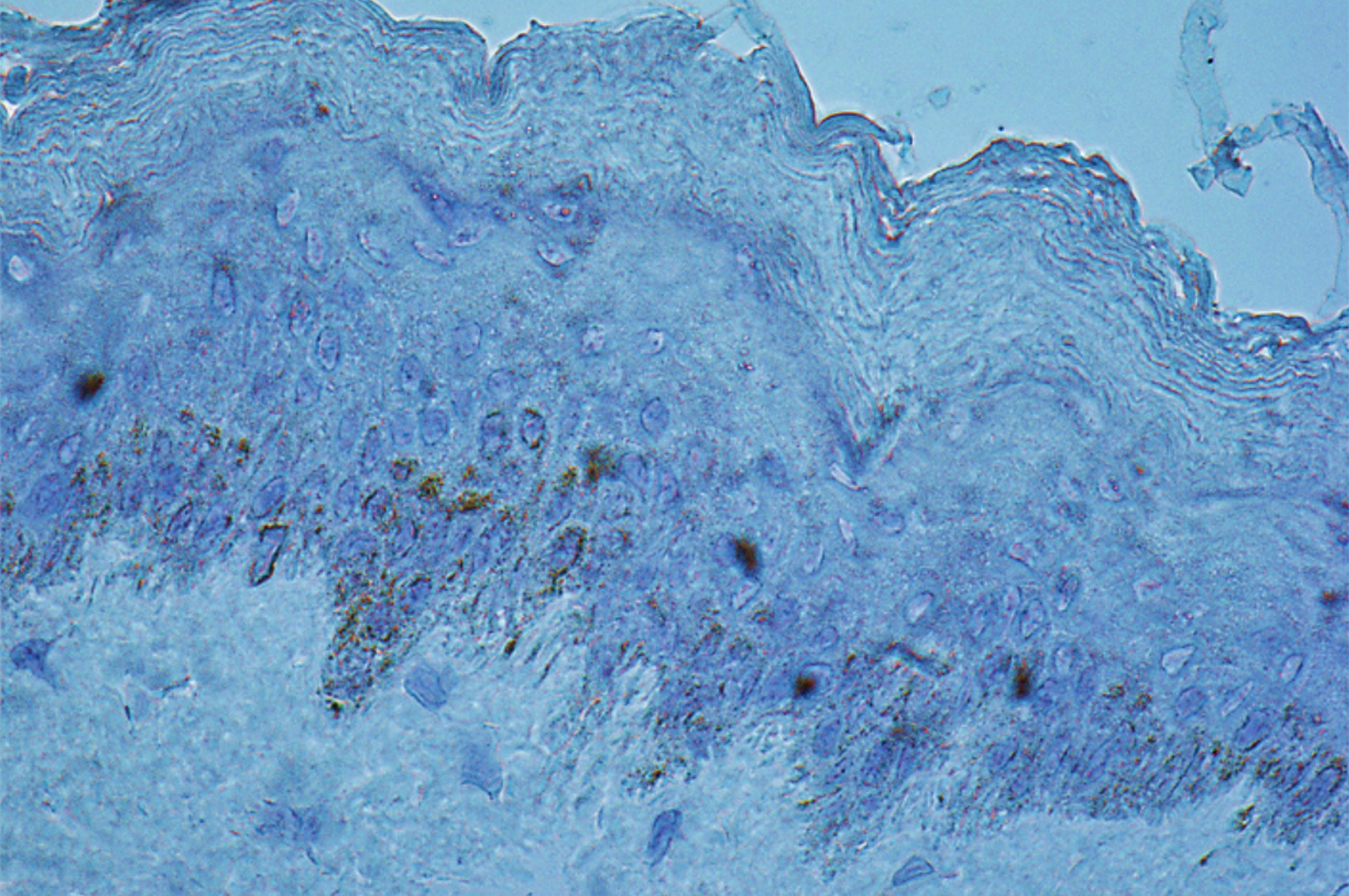
Les Kératoses Actiniques (KA) sont des lésions cutanées fréquentes, rugueuses à la palpation, et majoritairement présentes sur les zones photo-exposées. Leur prévalence aux USA et en Europe est estimée entre 11 et 25% de la population. En France, elles concernent 754/100.000 patients et représentent le premier motif de consultation en dermatologie. Elles atteignent plus volontiers les sujets âgés, de phototype clair, ayant travaillé à l’extérieur. Parfois douloureuses et hémorragiques au contact, il s’agit surtout de lésions ayant la capacité d’évoluer vers un carcinome épidermoïde invasif.
Les KA sont souvent multiples et la peau apparemment saine située entre les lésions présente des anomalies non visibles à l’œil nu mais mises en évidence à l’examen histologique et lors d’analyses biologiques (champ de cancérisation). On estime que pour un individu avec 7,7 KA, la probabilité qu’au moins une de ces lésions évolue vers un carcinome épidermoïde invasif sur une période de 10 ans est de 10%. Le potentiel malin et le caractère imprévisible de l’évolution des KA ont mené à un consensus sur la nécessité de les traiter.
La thérapie photodynamique (PDT) consiste en l’exposition à une lumière de longueur d’onde particulière de cellules tumorales préalablement photosensibilisées. En dermatologie, la photosensibilisation repose sur l’application topique de methyl-aminolévulinate (MAL) contenu dans la crème Metvixia® (Galderma SA). Appliqué sur la zone à traiter, cet agent pharmacologique induit l’accumulation spécifique du photosensibilisant, la Protoporphyrine IX (PpIX), dans les cellules tumorales.
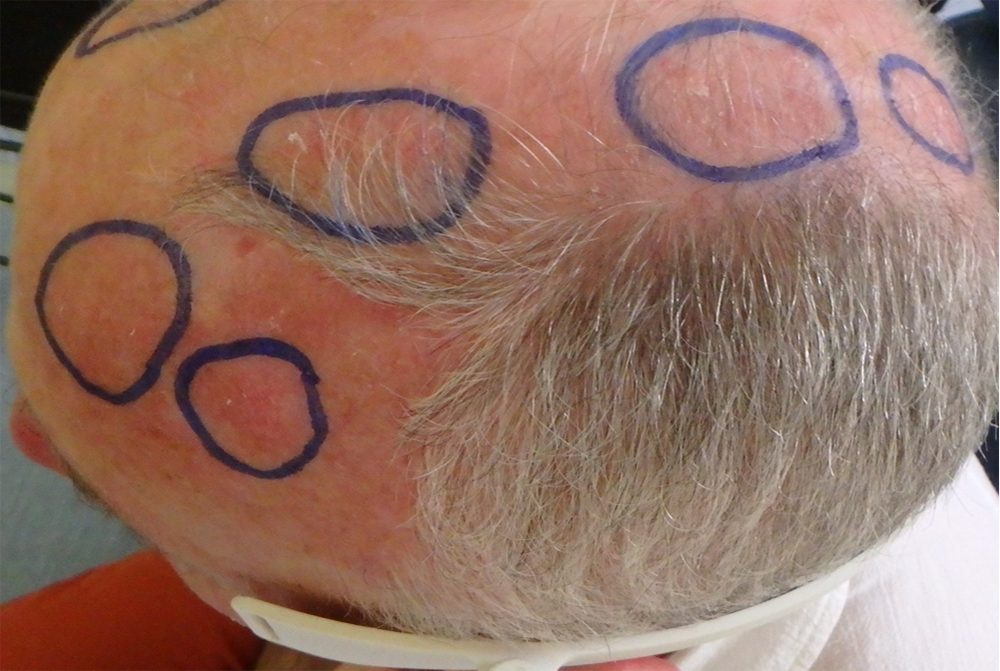
La source lumineuse la plus communément utilisée en Europe pour activer la PpIX est la lampe Aktilite CL 128 (Galderma SA). Cette lampe, constituée d’un panneau rigide de LEDs, émet une lumière rouge à une longueur d’onde de 630 nm et délivre une dose de lumière de 37J/cm² (75 mW/cm²).
Bien que souvent décrite comme très douloureuse par les patients, la PDT reste un traitement de premier choix pour la prise en charge des kératoses actiniques multiples car elle permet de traiter de larges zones avec un taux de réponse satisfaisant et d’excellents résultats cosmétiques.
Objectifs
L’objectif du programme DermatoPDT de l’unité ONCO-THAI est de développer de nouveaux dispositifs et protocoles d’illumination, qui devraient permettre de solutionner en partie ces limites.
Regroupant des plateformes techniques et logicielles, le programme intègre notamment des travaux de recherche sur la modélisation mathématique de l’interaction lumière - tissu biologique1 et le développement de logiciels permettant l’analyse et la comparaison de sources lumineuses2.
Illustration du spectre d’émission d’un dispositif classique d’illumination pour la PDT en dermatologie (en bleu), du spectre d’absorption normalisé de la PpIX (en vert), et de l’irradiance spectrale efficace (en violet).
Le programme de recherche DermatoPDT repose également sur le développement de nouveaux dispositifs, intégrant de nouvelles modalités d’illumination3.
Dans le cadre du projet ANR-12-EMMA-0018, l’unité ONCOTHAI a contribué au développement d’un nouveau dispositif d’illumination : Flexitheralight4.
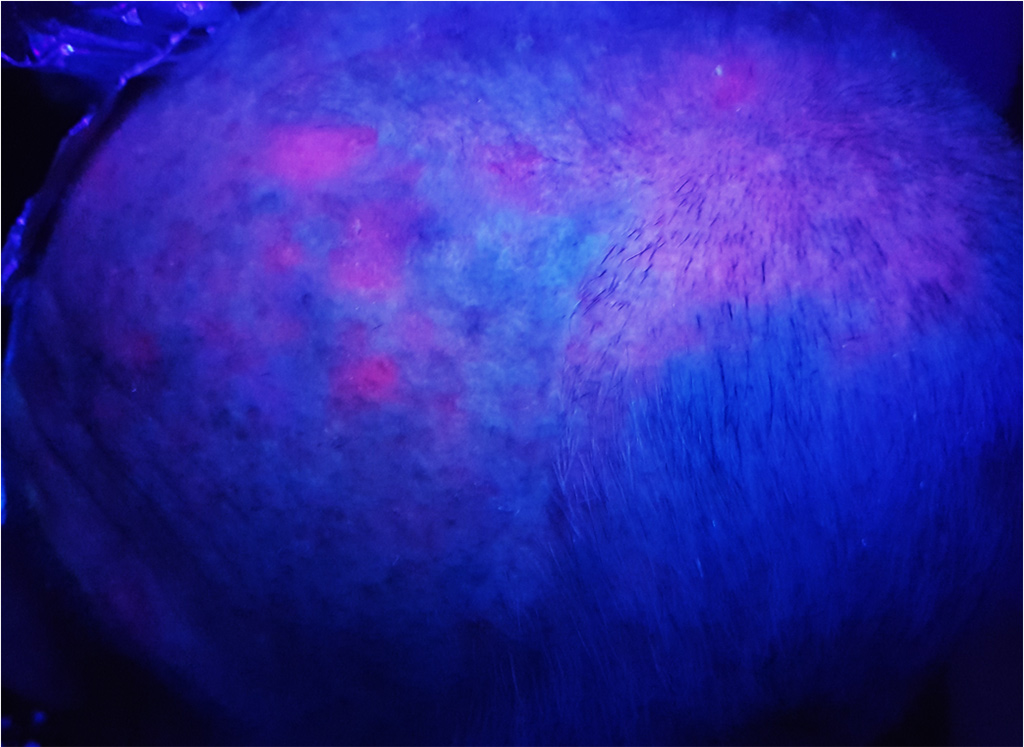
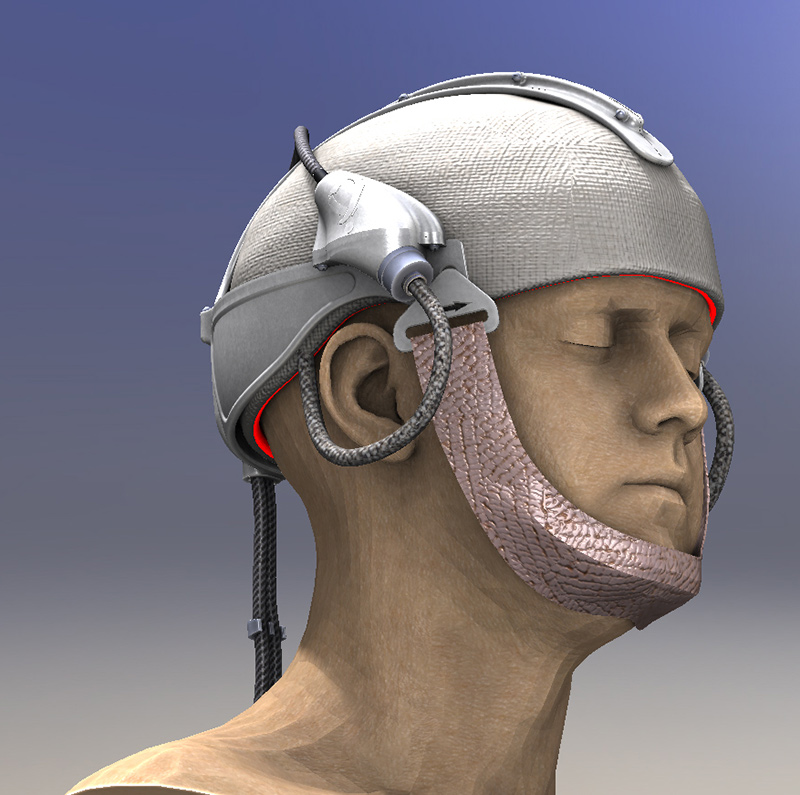
Basé sur l’utilisation d’un textile lumineux souple conformable à la complexité de l’anatomie humaine, il garantit une illumination homogène de l’ensemble des lésions (notamment au niveau du scalp). Par ailleurs, le textile lumineux diffuse une lumière rouge (635 nm), avec un débit de dose faible (12 mW/cm2) de façon à minimiser les douleurs habituellement ressenties par les patients.
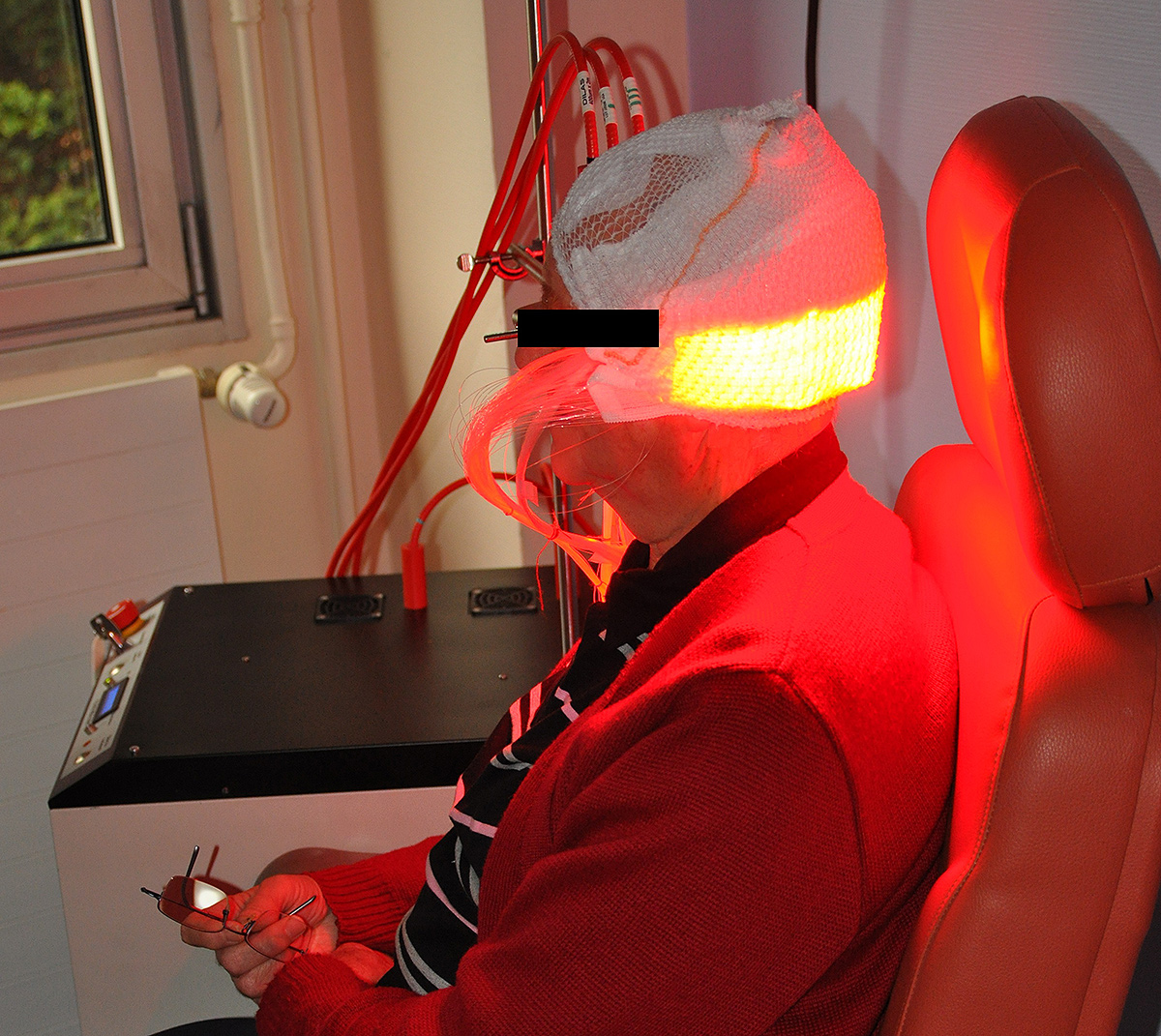
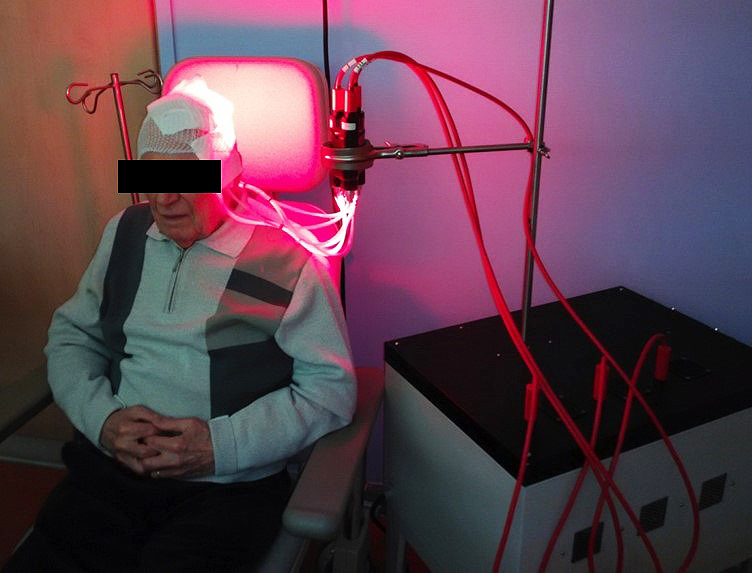
En 2013, l’unité ONCO THAI a initié le projet Européen CIP 621103 Phosistos, et son partenariat avec différents laboratoires et industriels européens, a abouti au développement d’un dispositif lumineux intégrant une technologie de textile lumineux mature, plus fonctionnelle et industrialisable5.
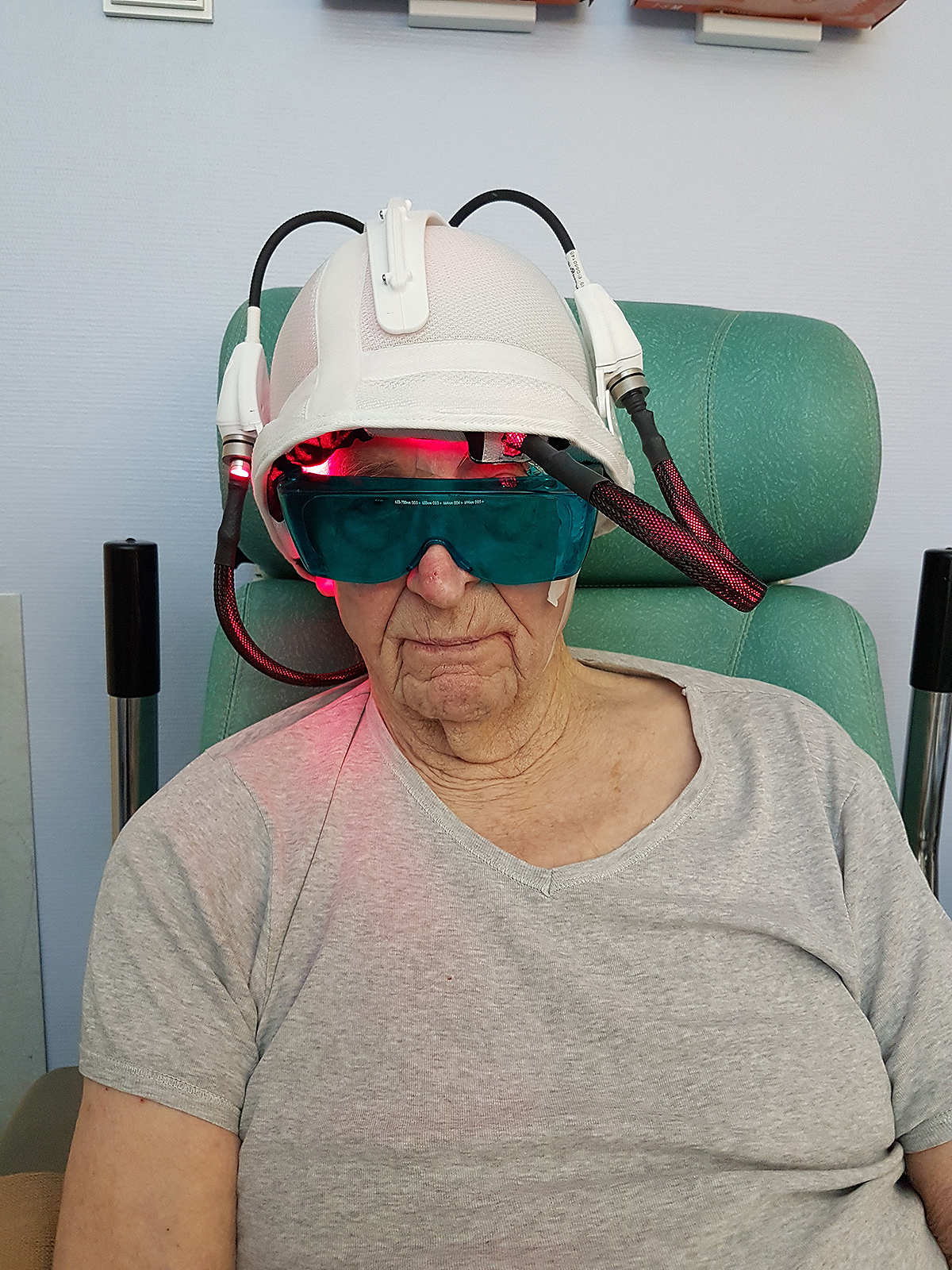
Où en sommes-nous ?
En 2016, le dispositif Phosistos6 a été évalué dans la prise en charge des kératoses actiniques au cours d’une étude de phase II, comparative, intra-individuelle, randomisée, menée au sein du service de dermatologie du CHU de Lille et celui de Klinikum Vest en Allemagne. Les hypothèses principales de cette étude étaient la non dangerosité du dispositif Phosistos et de la modalité d’illumination, la non-infériorité en termes d’efficacité et la meilleure tolérance par rapport à la PDT classique.
Une quarantaine de patients présentant au moins 10 KA a été inclus dans cette étude. Les kératoses actiniques étaient réparties en 2 groupes : le 1er groupe recevait la PDT classique (Aktilite CL 128 et un débit important : 75 mW/cm²) alors que le second groupe était traité avec le dispositif Phosistos. La réponse thérapeutique à 3 mois ainsi que la tolérance clinique, étaient évaluées pour les 2 méthodes, puis comparées.
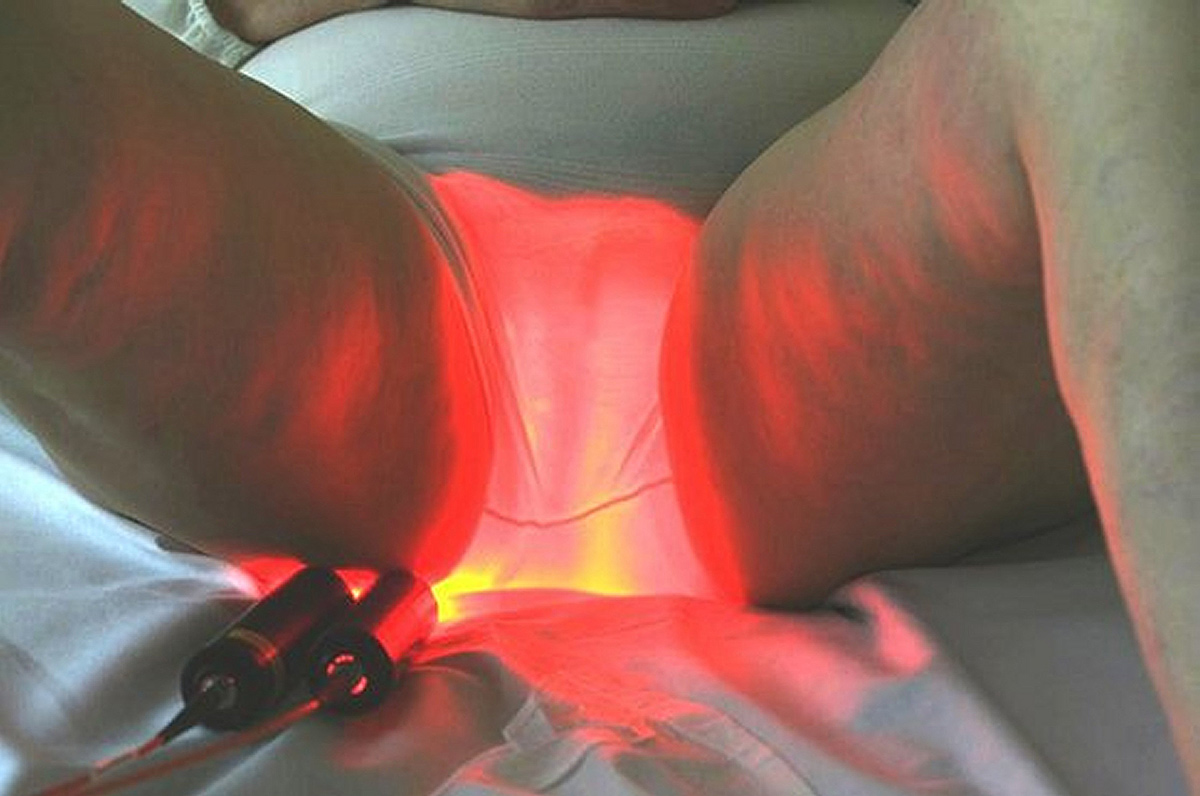
Les résultats montrent une efficacité du dispositif Phosistos comparable à la PDT classique, avec une douleur pratiquement nulle.
D’autres applications de ces dispositifs sont à l’étude, comme le Paget Extra-Mammaire, ou la Folliculite décalvante.
La technologie des textiles lumineux peut être associée à différentes sources de lumières et permet de délivrer différentes modalités d’illumination, en s’adaptant aux contraintes réglementaires (comme l’utilisation du Levulan® aux Etats-Unis, qui requiert une illumination à 417 nm) et cliniques.

1 Vignion-Dewalle, A.S., et al., Comparison of three light doses in the photodynamic treatment of actinic keratosis using mathematical modeling. J Biomed Opt, 2015. 20(5) : p. 58001.
2 Vignion-Dewalle, A.S., et al., A software for analyzing and comparing the light sources available for PDT in dermatology. EuroPDT Munich, 2017
3 Mordon, S., et al., Light emitting fabric technologies for photodynamic therapy. Photodiagnosis Photodyn Ther, 2015. 12(1) : p. 1-8
4 Etude de phase II évaluant la non-infériorité du dispositif Flexitheralight par rapport à la photothérapie dynamique (PDT) classique* : n° 2013-A01096-39* – ID clinical trial : NCT03076918
5 (www.phosistos.com)
6 Etude de phase II évaluant la non-infériorité du dispositif Phosistos par rapport à la photothérapie dynamique (PDT) classique : n° 2016-A00010-51 – ID clinical trial : NCT03076892
Besoin de plus d'informations sur DermatoPDT ? Contactez-nous
Contexte et enjeux
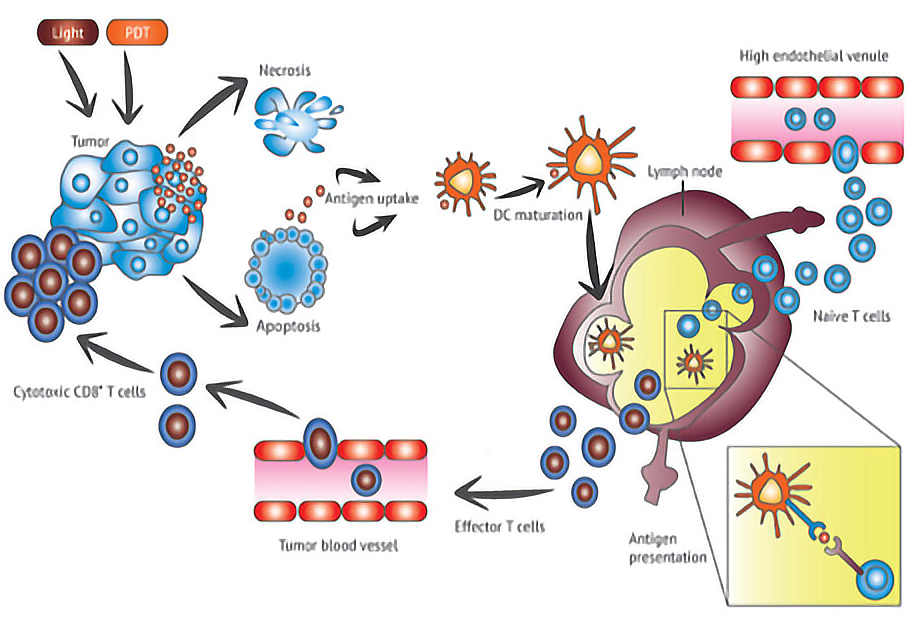
L’utilisation de la PDT dans le domaine de l’oncologie a déjà fait ses preuves et connait depuis ces dernières années un intérêt grandissant. Aujourd’hui, il existe un réel rationnel pour penser que la PDT pourrait impacter la réponse immunitaire, en faveur d’une immunoactivation. Cette propriété serait un atout considérable dans la prise en charges des cancers si l’on prend en considération le succès de certaines immunothérapies anti-tumorales (anti-PD1, PDL1, CTLA-4…), en particulier depuis ces 3 dernières années.
Au sein de l’unité Oncothai, l’équipe ImmunoPDT travaille en étroite association avec l’équipe PhysicoPDT dirigée par le Dr Maximilien Vermandel, et en collaboration avec les cliniciens du CHRU de Lille et du Centre Oscar Lambret. Les 5 principaux projets développés au sein de l’équipe ont pour ambition de mieux comprendre l’impact de la PDT sur la réponse immunitaire en évaluant plus spécifiquement les mécanismes impliqués dans l’immuno-modulation du système immunitaire par la PDT.
La réalisation de ces projets nécessite de s’appuyer sur une double expertise, celle acquise historiquement par l’équipe « Immunorégulation des Cancers Viro-induits » dirigée par le Pr Nadira Delhem, dans les domaines de l’immunosurveillance et de l’immunothérapie des cancers, et celle acquise par l’équipe "Physico PDT" dans le domaine des lasers et de la thérapie photodynamique. C’est en effet, la synergie de ces compétences qui permettra de comprendre en amont le rôle de la PDT dans la régulation immunitaire, afin de proposer des protocoles innovants dans le traitement des cancers.
Objectifs
L’unité INSERM U1189, en collaboration avec les services cliniques de Gynécologie, de Transplantation digestive, de Neurochirurgie, de Dermatologie et de Pneumologie du CHRU de Lille, ont débuté 5 projets ambitieux visant à évaluer, en parallèle de l’efficacité de la PDT entant que traitement anti-tumoral, l’impact de la PDT sur la régulation de la réponse immunitaire. Ces travaux se déroulent sous deux versants : clinique et recherche. Sur le plan Recherche, l’équipe immunoPDT propose de développer des projets fondamentaux plus en amont de la recherche translationnelle, visant à comprendre au niveau biologique et moléculaire, l’impact de la PDT, à la fois sur les cellules tumorales et sur les cellules immunitaires [Projets IM-PRODYNOV (carcinose ovarienne) et HEPATOCAR (hepatocarcinome)].
Par ailleurs, l’équipe ImmunoPDT a développé des outils méthodologiques et techniques performants dans l’évaluation in vivo de nouvelles stratégies thérapeutiques anti-tumorales.
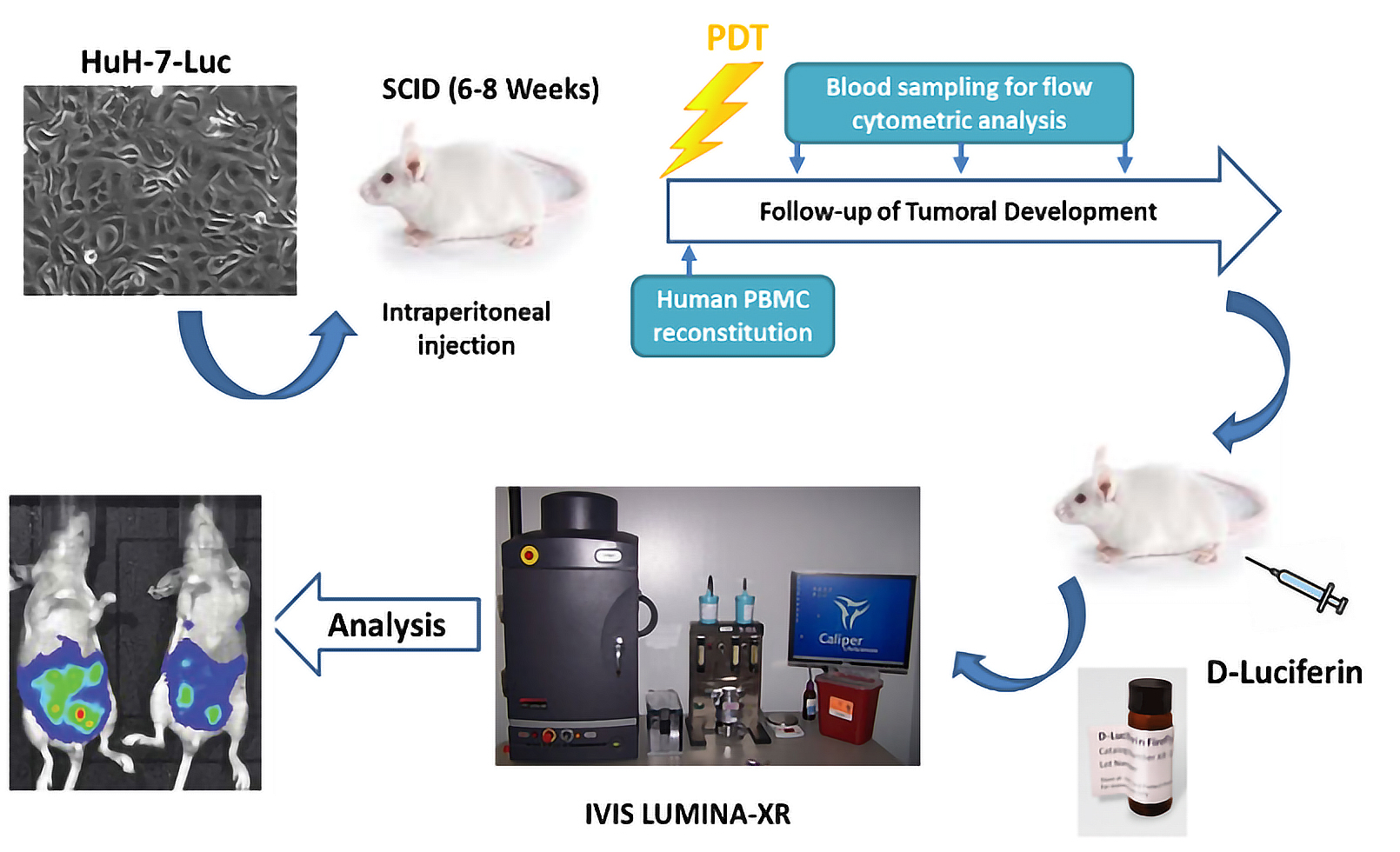
L’équipe a notamment mis au point des modèles innovants de souris humanisées « à façon » qui associent la xeno-transplantation de tumeurs humaines exprimant la luciférase, à la reconstitution avec un système immunitaire humain complet. Ces modèles, facilement exploitable en imagerie du petit animal, permettent de développer des stratégies anti-tumorales dans un contexte très proches de la physiopathologie humaine.
Afin d’évaluer dans ces modèles in vivo, l’efficacité de la PDT et son impact sur un système immunitaire humain, l’unité U1189 a développé des dispositifs innovants d’illumination in vivo des souris.

Sur le plan clinique, l’équipe ImmunoPDT développe des projets de recherche plus translationnels visant à caractériser les effets de la PDT, combinée à la chirurgie ou à l’immunothérapie, sur le phénotype et l’activation des cellules immunitaires (immunomonitoring) et sur la régulation de la réponse immunitaires (lymphocytes T régulateurs, DC tolérogènes, exosomes tumoraux…). L’ensemble de ces études sont réalisées à partir de prélèvements issus de patients inclus dans des essais cliniques ou des études ancillaires [Projets IM-INDYGO (glioblastome), IMCUTALA (mélanome) et IMPALA (mesothéliome)].
Où en sommes nous ?
Grâce au soutien financier de la SATT Nord de France et Grand-Est, un brevet sur un nouveau photosensibilisateur (PS), ciblant spécifiquement des carcinoses ovariennes péritonéale, a été déposé. Le photosensibilisateur (PS-FOL) présenté ici est le produit d’une synthèse originale réalisée par l’équipe du Laboratoire de Réactions et Génie des Procédés (LRGP - UMR 7274 CNRS - Université de Lorraine). L’objectif de cette synthèse est d’associer le photosensibilisateur (PS) à une molécule d’adressage (acide folique) ciblant FR avec une forte affinité. Nous ne pouvons détailler davantage la nature de ce composé pour des raisons de confidentialité.
Notre objectif principal était d'évaluer la PDT dans cette indication, ainsi que son impact sur la réponse immunitaire. Les premiers résultats in vitro ont montré l’excellente efficacité de la PDT sur les lignées cellulaires humaines de carcinome ovarien.
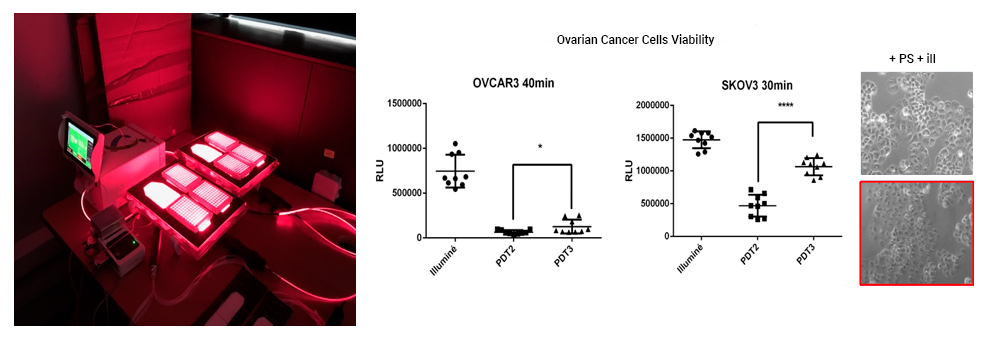
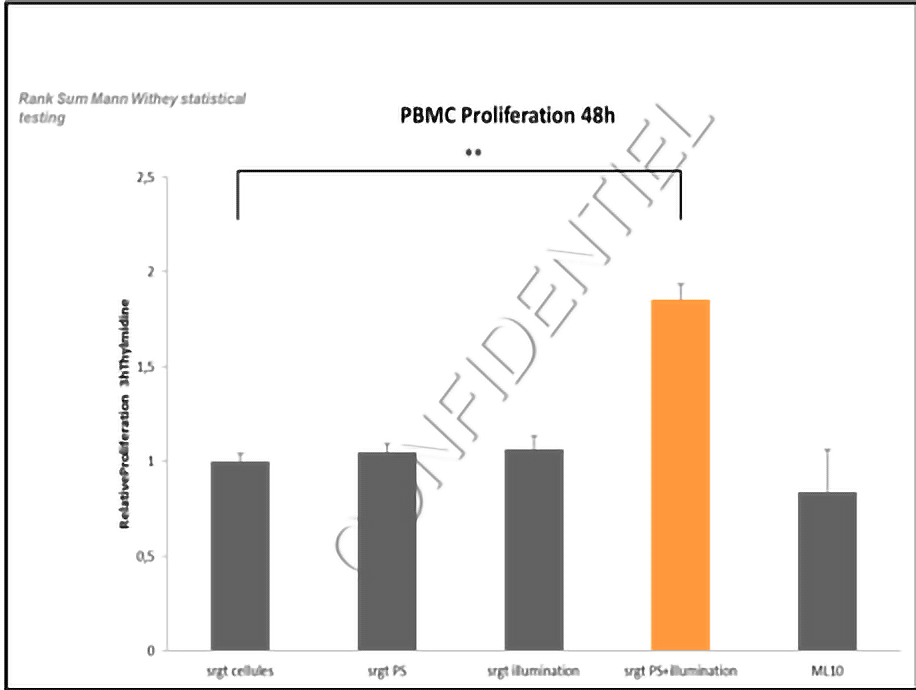
Par ailleurs, la PDT a également un effet bénéfique sur le système immunitaire. Les résultats observés montrent que les cellules tumorales soumises à la PDT produisent des facteurs favorisant l’immunostimulation en induisant une augmentation de la prolifération des cellules immunitaires humaines. La PDT permet également d’induire une diminution de la production de cytokines pro-inflammatoires par les cellules tumorales et une augmentation de cytokine favorable à la survie et la prolifération et l’activation des cellules immunitaires telles que les cytokines IL2, IFN-gamma et les cellules lymphocytaires T CD4+ et T CD8+.
Dans le contexte des carcinomes hépatocellulaires (PDT), nous avons pu obtenir des premiers résultats très prometteurs grâce à l’obtention d’un financement de thèse international. L’objectif principal de cette étude est de comprendre, dans le contexte du CHC, les effets directs et indirects de la PDT médiée par l’Acide 5-Aminolevulinic (5-ALA). Dans ce contexte, des lignées cellulaires de cancer hépatique ont été utilisées dans un premier temps : HuH7 (surexprimant p53), Hep3B (délétion partielle de p53) et HepG2 (exprimant p53 sauvage) et dans un second temps des cellules primaires de CHC issues d’exérèse chirurgicale seront utilisées.
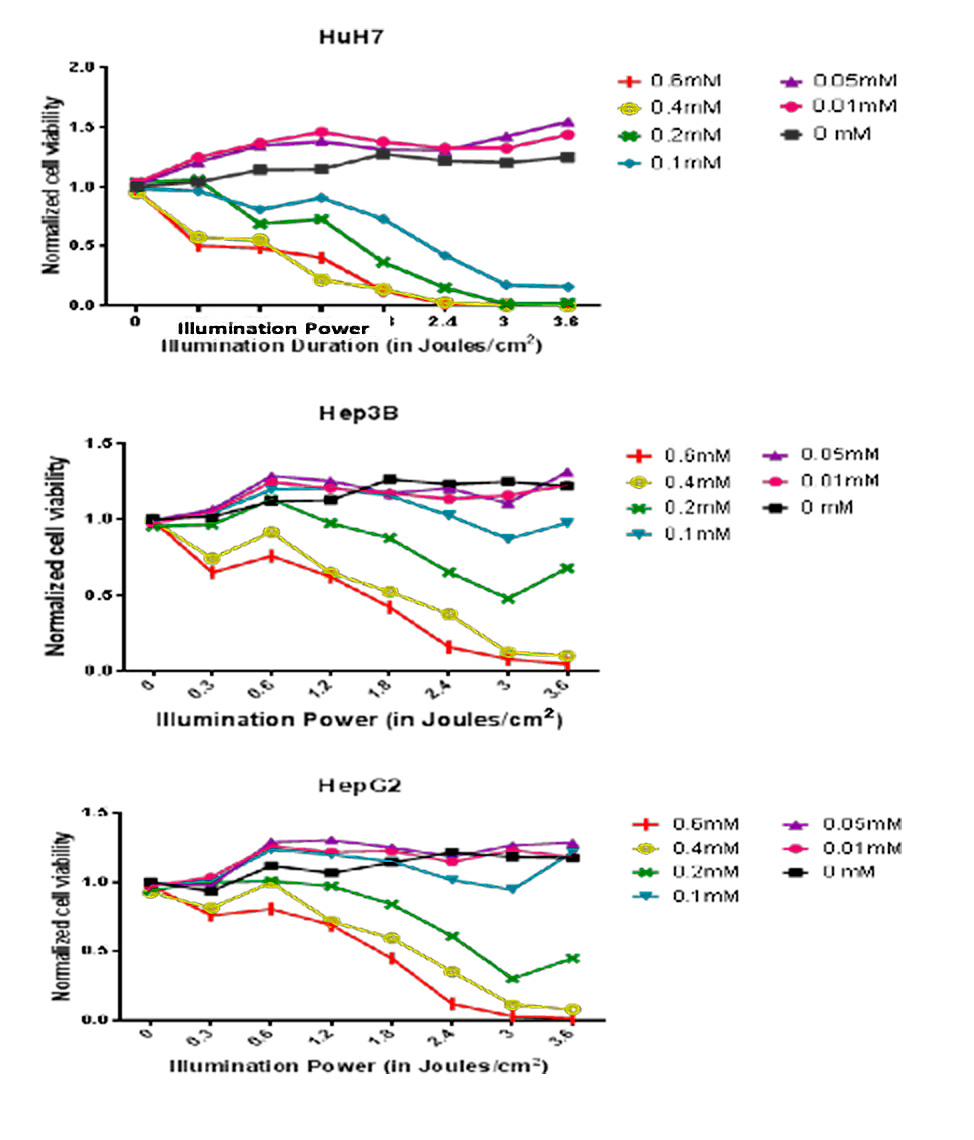
Nos résultats préliminaires ont démontré que la PDT peut être efficace contre les trois lignées cellulaires différentes de CHC car elles expriment les enzymes clefs responsables de la conversion de la pro-drogue 5-ALA en Porphyrine IX (PpIX), le PS final.
Ainsi, le traitement par PDT au 5-ALA de ces lignées, induit une mort cellulaire dépendante de la dose de 5-ALA et de la durée d’illumination.
De façon intéressante, nous avons également observé que ces trois lignées cellulaires répondent de manière variable à la PDT par 5-ALA selon un schéma qui semble lié au profil d’expression de p53.
Par ailleurs, grâce à un réseau de collaboration très étroit avec des cliniciens du CHRU de Lille et du centre Oscar Lambret et grâce au soutien soutien logistiques et financiers d’industriels (Novartis, BMS et MSD), nous avons initié 2 nouveaux projets dans le cadre du Mélanome et des mésothéliums. Les immunothérapies, comme les anticorps anti-PD-1, sont apparues ces dernières années comme un outil thérapeutique majeur dans de nombreux cancers. Ainsi, les avantages apportés à la fois par l’immunothérapie et la PDT nous ont conduits à proposer une combinaison des deux traitements afin d’améliorer l’effet anti-tumoral local chez des patients présentant un mélanome avec métastases cutanées, ou présentant des mésothélium.
Sur la base d’un rationnel d’effet synergique de la PDT et des inhibiteurs de checkpoint immunitaires, nous espérons induire une forte réponse immunitaire anti-tumorale, en l’absence de toxicités cumulatives et menant à une meilleure issue pour ces patients.
Besoin de plus d'informations sur ImmunoPDT ? Contactez-nous
Contexte et enjeux
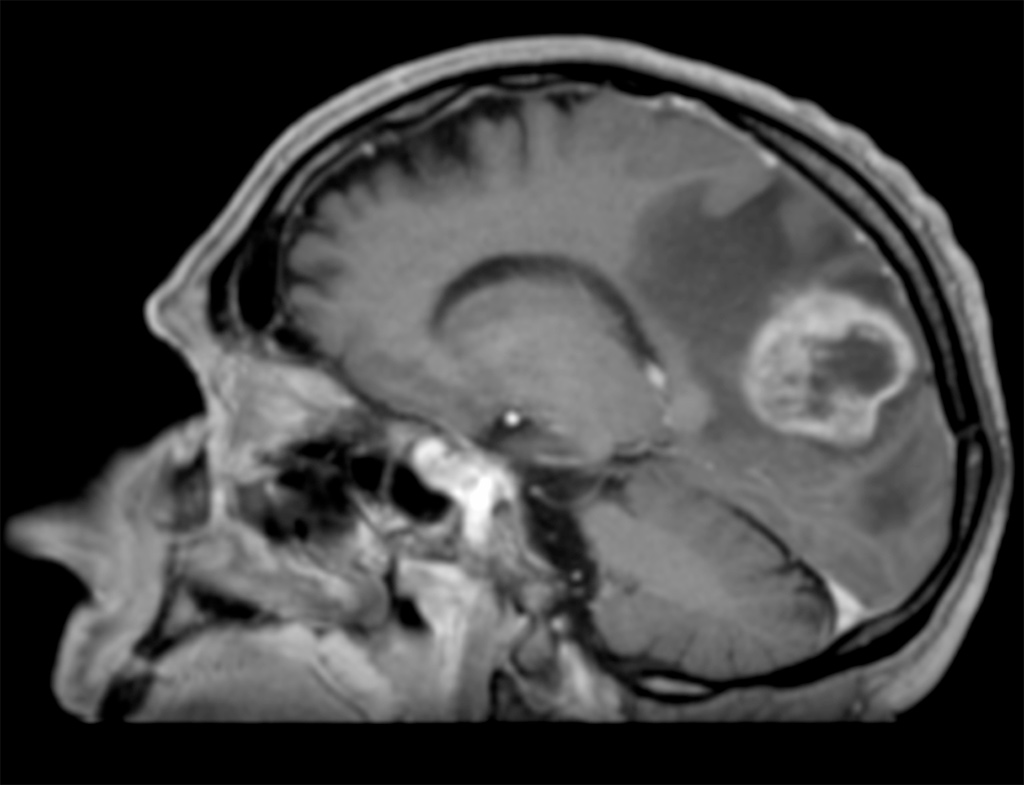
Avec environ 2 400 nouveaux cas par an en France, le glioblastome est la 3e cause de décès par cancer chez le jeune adulte (entre 15 et 35 ans). Il s’agit d’une tumeur incurable dont la médiane de survie est inférieure à 18 mois. La plupart des patients décèdent dans les deux ans. Ce domaine de l’oncologie est l’objet de nombreux travaux de recherches fondamentale et clinique. Le traitement de référence s’appuie sur la chirurgie, la radiothérapie cérébrale et la chimiothérapie.
L’objectif de la chirurgie est d’obtenir une réduction maximale du volume tumoral sans altérer le pronostic fonctionnel des patients compte tenu de leur pronostic vital péjoratif. Néanmoins, même en cas de traitement chirurgical satisfaisant, le caractère invasif et rapidement proliférant du glioblastome ne permet pas son contrôle par les protocoles thérapeutiques conventionnels. De fait, les patients, dont la localisation tumorale ne permet pas la chirurgie, présentent une survie limitée.
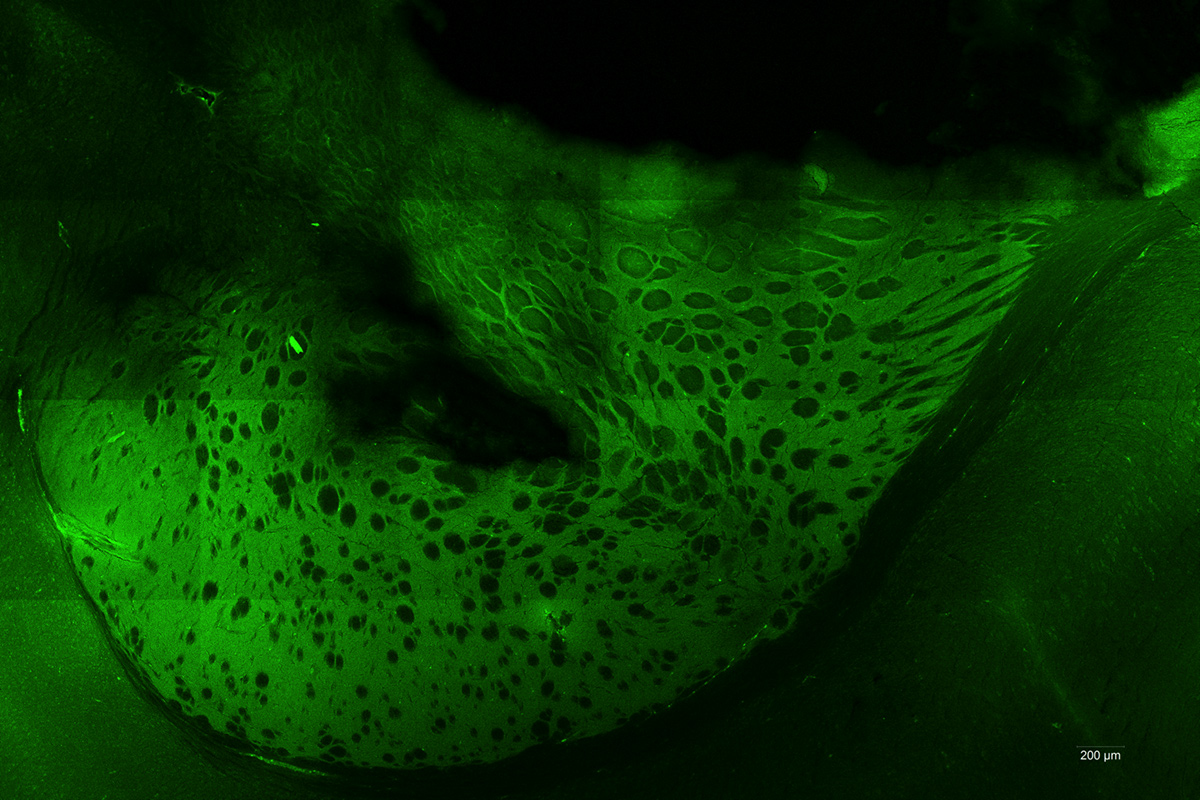
La thérapie photodynamique (PDT) consiste en l’exposition à une lumière laser de cellules tumorales photosensibilisées par l’administration générale ou locale d’un agent pharmacologique. Nos recherches s’articulent autour de l’acide 5-Aminolévulinique (5-ALA) qui induit une accumulation relativement spécifique d’un photosensibilisant : la protoporphyrine IX (PPIX). Ce photosensibilisant, qui est présent uniquement dans les cellules tumorales, entraîne leur destruction spécifique lors de l’illumination tout en permettant de préserver les tissus sains.
L’objectif du programme NeuroPDT de l’unité Onco-ThAI est de développer un schéma de thérapie photodynamique efficace, reproductible et sélectif, utilisant le 5-ALA. Aujourd’hui, le travail expérimental semble confirmer l’efficacité de la thérapie laser 5-ALA ainsi que l’innocuité de son mode d’administration. Cette thérapie devrait ainsi rapidement faire l’objet d’applications en clinique humaine. Notamment grâce au même principe actif déjà utilisé pour visualiser la tumeur lors de la chirurgie des gliomes.
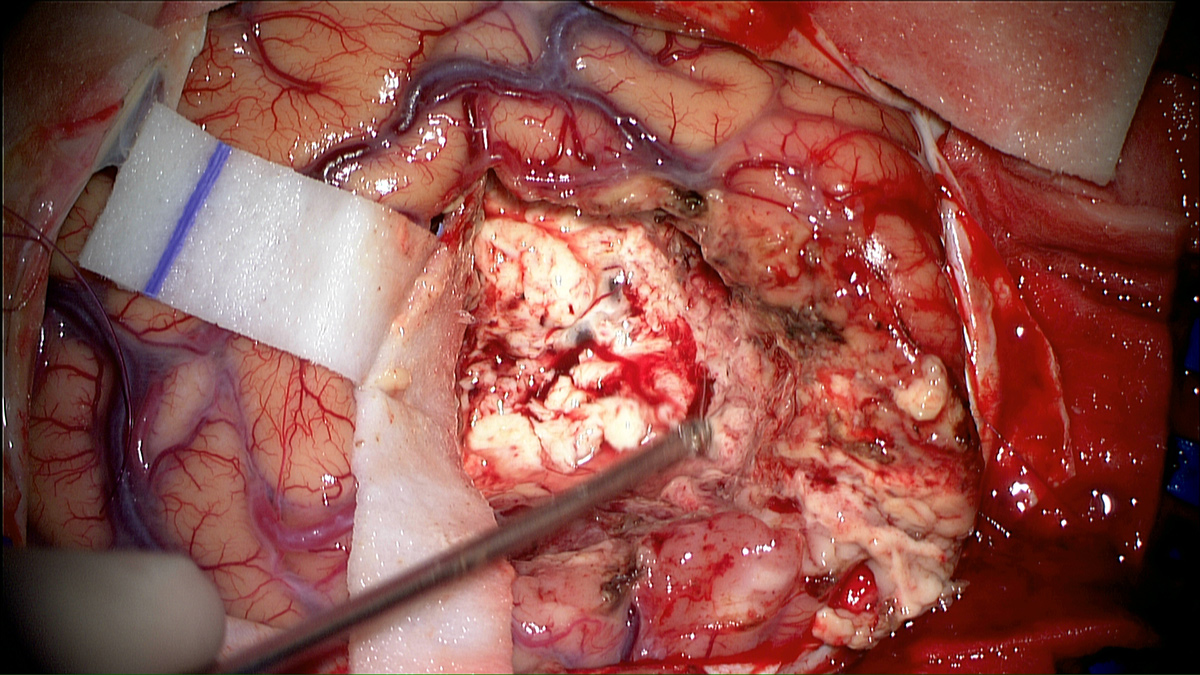
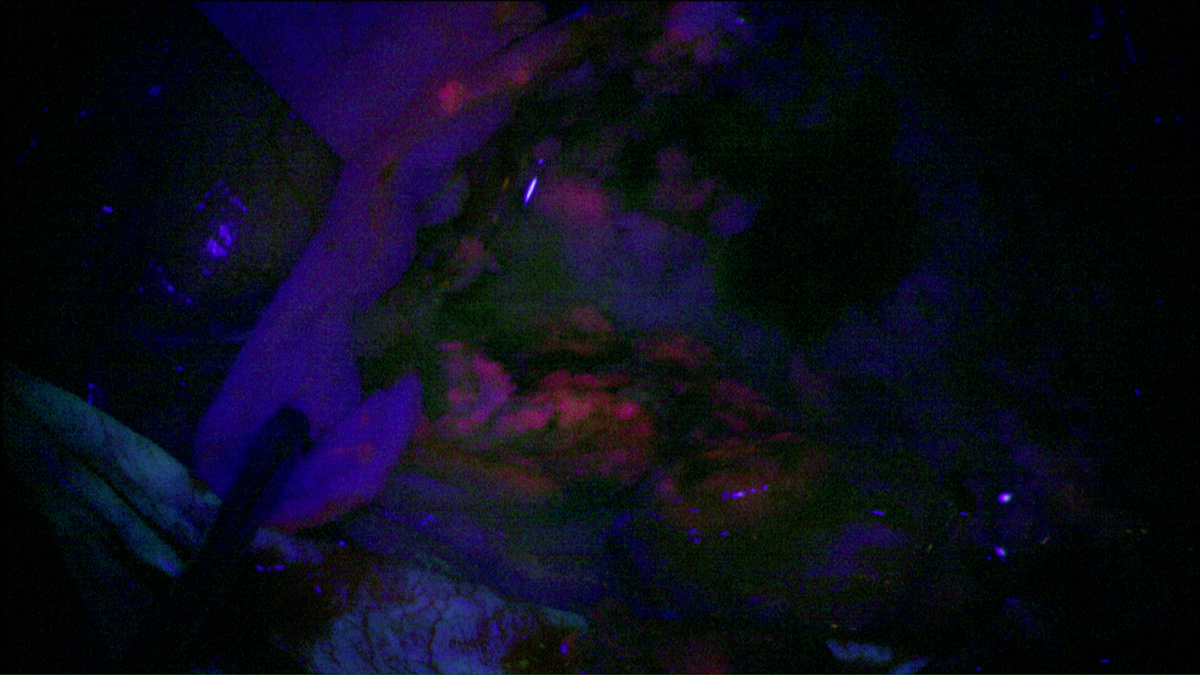
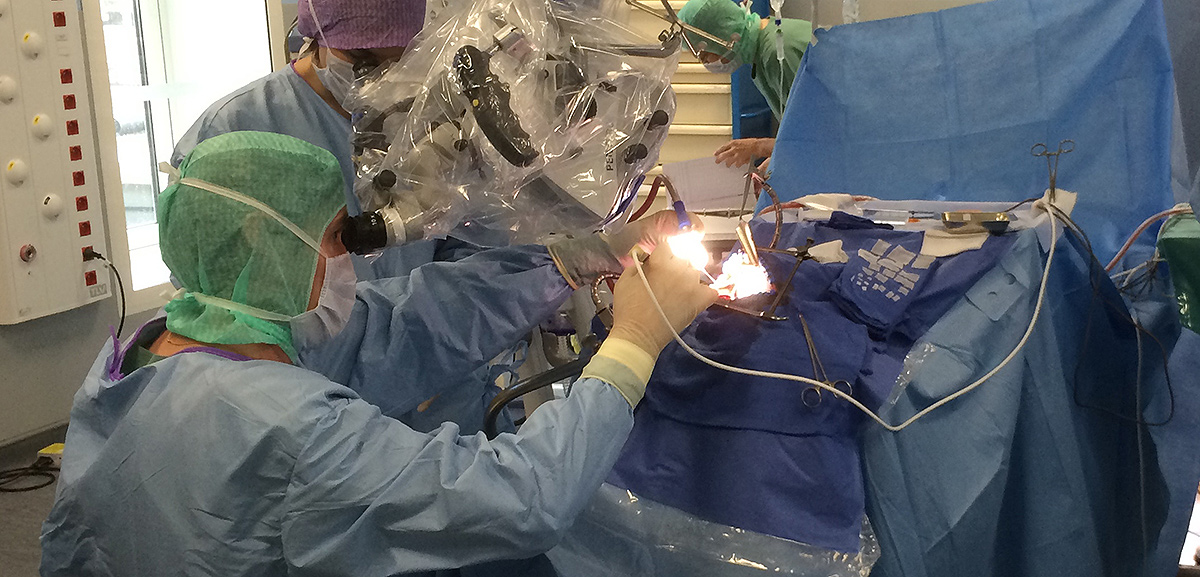
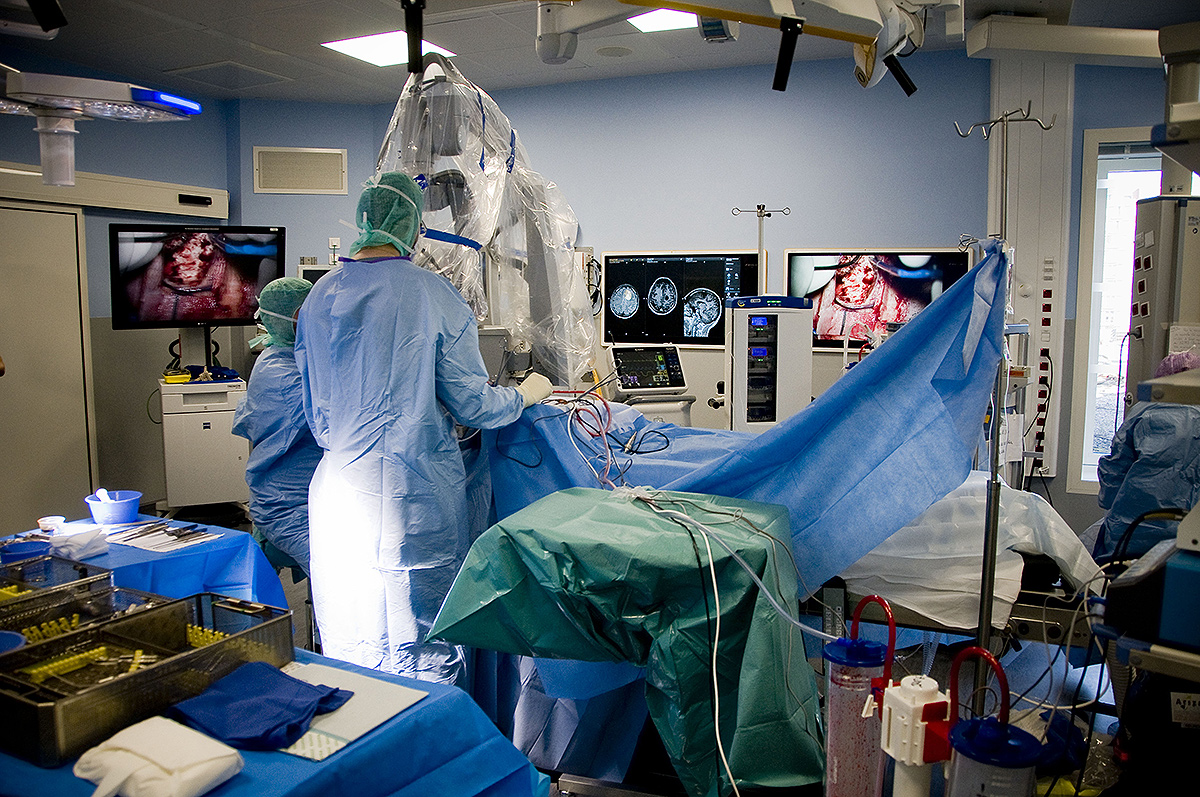
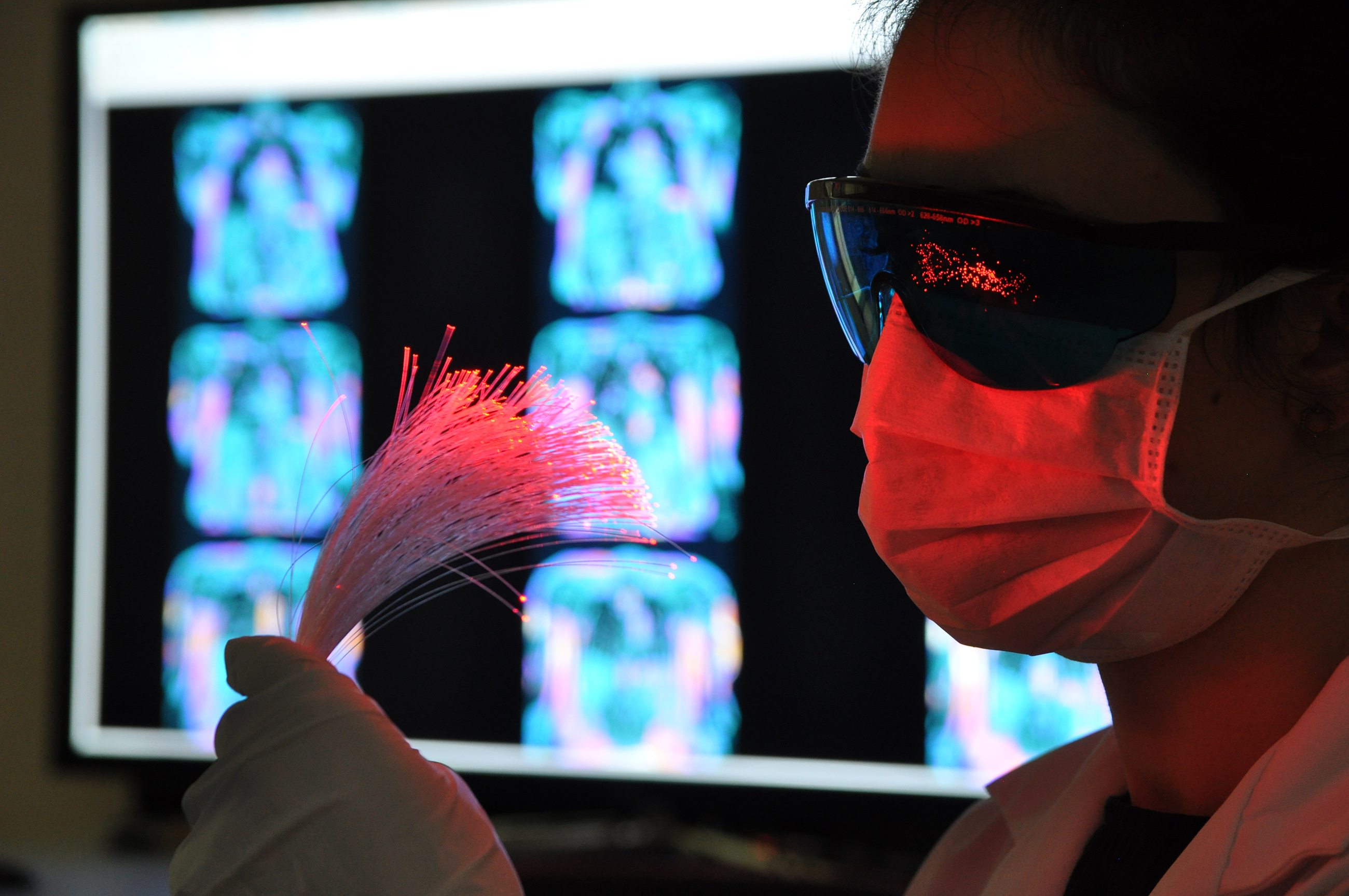
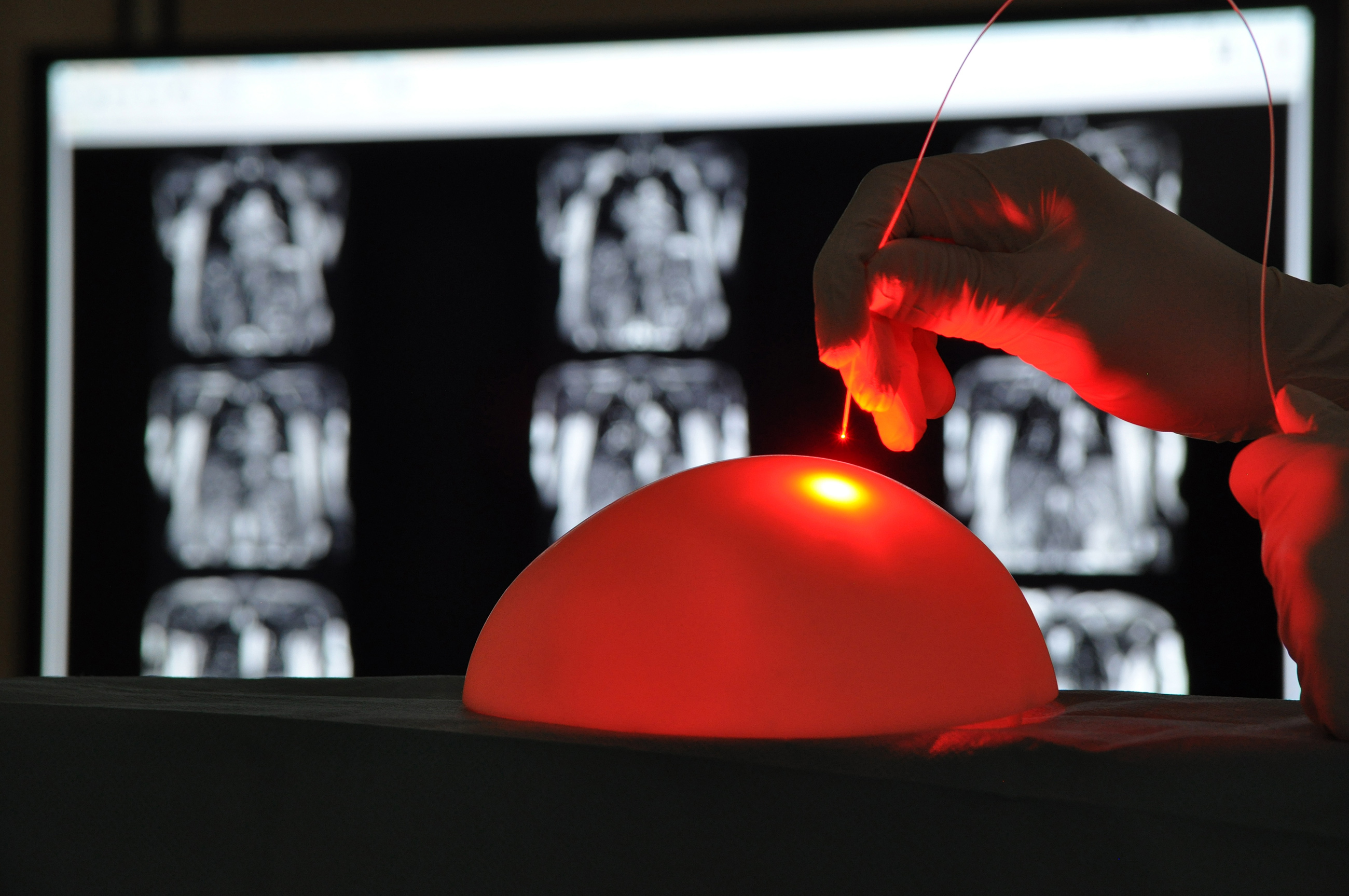
Dans un contexte de thérapie, l’illumination des cellules photosensibilisées peut-être produite selon deux procédés : l’exposition à une lumière rouge du foyer opératoire pendant l’intervention ou l’insertion de fibres optiques intracérébrales, dans le cas d’un traitement à distance de la chirurgie. Cette dernière solution pourrait, par ailleurs, représenter une option thérapeutique décisive pour les patients présentant un glioblastome inopérable ou en récidive. L’évaluation de ce développement clinique fait actuellement l’objet d’un programme de recherche clinique.
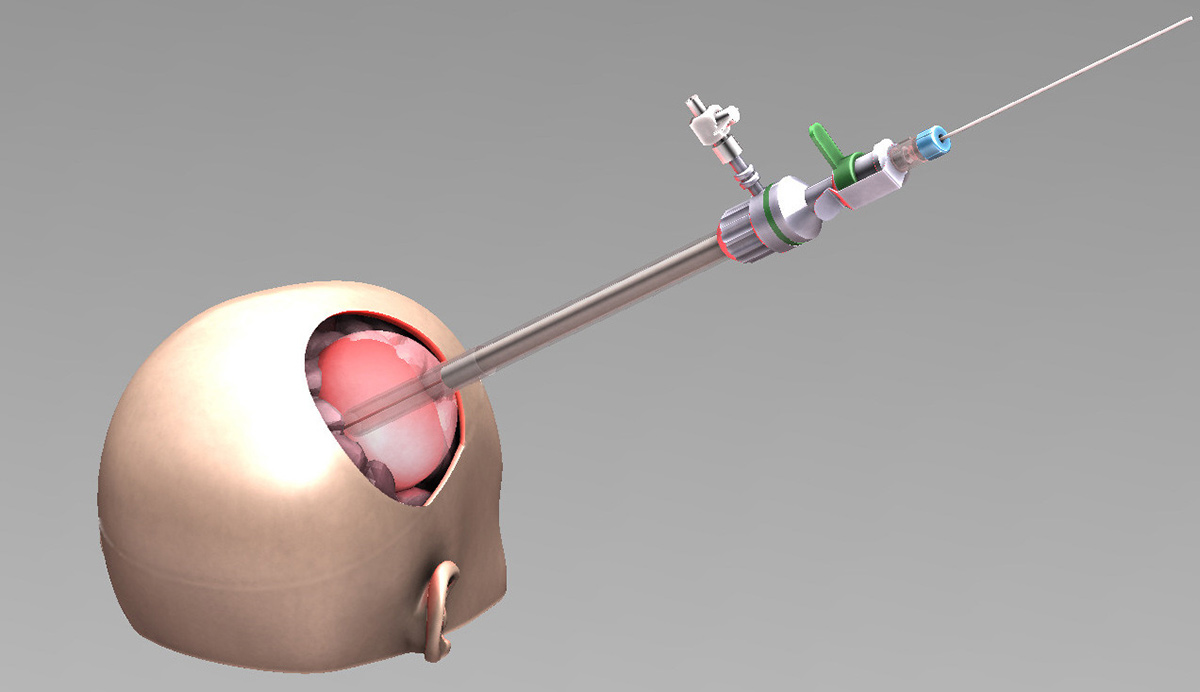

A terme, les résultats attendus sont ceux d’une amélioration significative de la survie consécutive à une diminution sélective de la tumeur, contrôlée par Imagerie par Résonnance Magnétique.
Objectifs
La finalité du projet est de proposer deux modalités distinctes de traitement : thérapie photodynamique peropératoire (perPDT) et thérapie photodynamique interstitielle (iPDT). En effet, ces deux solutions sont complémentaires puisque la perPDT est un complément thérapeutique prometteur pour enrichir l’arsenal thérapeutique actuel (chirurgie-radiothérapie-chimiothérapie) et l’iPDT constitue une modalité nouvelle pour la prise en charge des glioblastomes non-opérables.
Inclure ces solutions dans la prise en charge du patient nécessite de décomposer la recherche en plusieurs étapes : étude préclinique – étude clinique – développements méthodologiques.
Une étude pré-clinique a été réalisée au laboratoire en vue de valider les hypothèses d’efficacité et d’optimiser la stratégie de traitement PDT.
Des fibres optiques couplées à une diode laser ont permis une illumination focalisée de la zone tumorale in-vivo. Ainsi, nous avons été en mesure de vérifier la réponse du glioblastome au traitement PDT. Sur un autre plan, cette étude nous a permis d’optimiser les modalités de traitement, de maîtriser l’ensemble des éléments de la chaîne de traitement (planification – traitement – suivi) et finalement de valider la preuve de concept de la PDT.
Les développements méthodologiques concernent à la fois le traitement de l’image et les modalités de traitement en iPDT ou perPDT.
Aujourd’hui, une étude approfondie des techniques d’imagerie est mise en place afin de définir les meilleures solutions pour la planification, le guidage et le suivi du traitement. Le panel d’imagerie étudié concerne à la fois l’imagerie métabolique par Tomographie par Emission de Positons (PET) et l’IRM.
Dans ce contexte, des algorithmes de segmentation en TEP sont développés de manière à quantifier précisément l’activité métabolique de la tumeur. Cette étape est primordiale car l’imagerie TEP combinée aux images IRM utilisées lors du diagnostic permettra de mieux définir les limites de l’envahissement tumoral et ainsi adapter la méthodologie de traitement et mieux cibler la thérapie.
Où en sommes nous ?
Les études cliniques doivent permettre de valider l’ensemble des développements mis en œuvre pour délivrer de façon optimale le traitement.
Aujourd’hui, une étude clinique pilote monocentrique est en cours de réalisation au CHU de Lille afin de démontrer la faisabilité d’une part, et l’innocuité du traitement peropératoire d’autre part. Cette étude, INDYGO (Intraoperative photodynamic therapy of glioblastoma) vise à délivrer la thérapie photodynamique lors de la chirurgie du glioblastome grâce un dispositif développé au laboratoire.
Sur le volet international, ONCO-THAI coordonne un réseau européen : SYNAPS (Synergizing Photodynamic Therapies for Neurosurgery). Ce réseau s’appuie sur un partenariat entre services de neurochirurgie, équipes de recherche et industriels des technologies de la santé. L’objectif de SYNAPS est d’aboutir à un essai clinique multicentrique et randomisé à travers l’Europe.
Finalement, ces travaux permettront de lever les verrous limitant l’utilisation de cette technique pour le traitement de ces tumeurs toujours incurables. Le traitement laser PDT pourrait rapidement compléter l’arsenal thérapeutique pour la prise en charge des glioblastomes, voire même devenir une nouvelle solution thérapeutique pour les localisations tumorales inopérables.
Besoin de plus d'informations sur NeuroPDT ? Contactez-nous
Contexte et enjeux
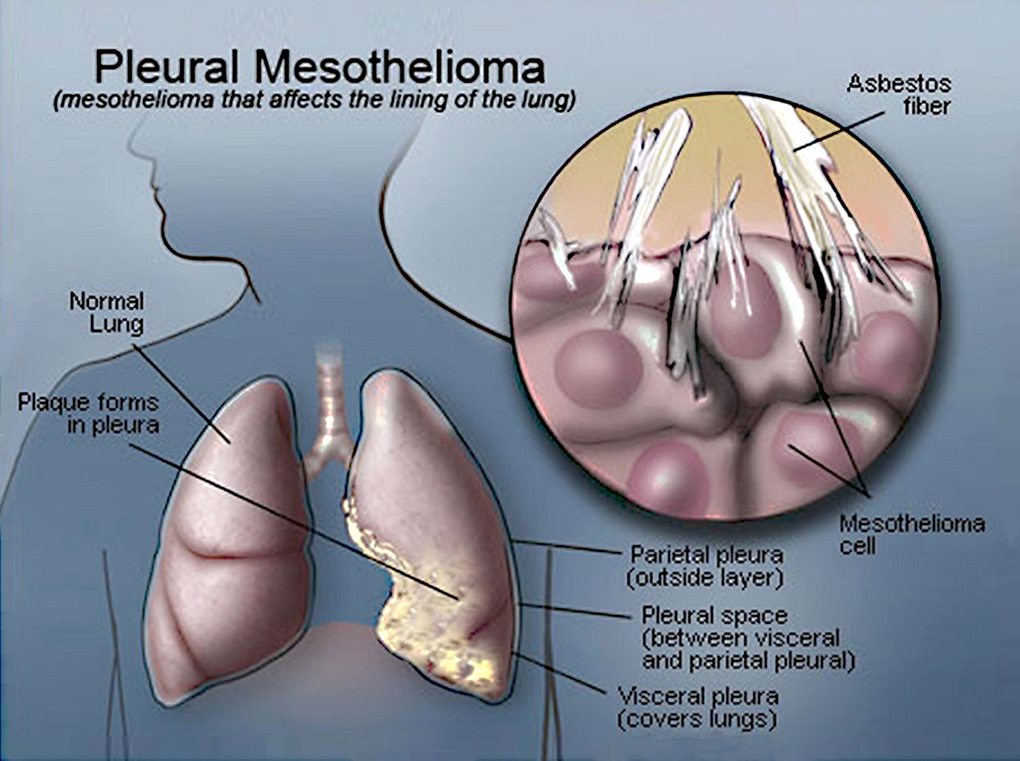
Autrefois considéré comme un cancer rare, le mésothéliome pleural malin (MPM), ou cancer primitif de la plèvre, représente aujourd’hui un enjeu important. Son pronostic est sombre (médiane de survie <1 an dans la littérature) et son incidence croissante depuis 1945 (due au large recours à l’amiante, son facteur étiologique principal, en France dans les années 1970-1980 jusque son interdiction en 1997). De nos jours, en France, l’incidence annuelle du MPM est d’environ 900 cas. Compte tenu du délai de latence habituellement long entre l’exposition de l’amiante et le diagnostic du mésothéliome (en moyenne de 30 à 40 ans), un pic d’incidence du MPM est attendu au cours de la prochaine décennie. Il serait déjà atteint dans certains pays (USA, Europe du Nord…) qui ont interdit l’utilisation de l’amiante précocement par rapport à la France. Cependant, de nombreux autres pays émergents (Chine, Brésil, Russie, Inde…) ou en voie de développement, extraient encore de l’amiante et/ou y ont recours de manière importante. Cela laisse craindre une probable « endémie » mondiale du mésothéliome pleural malin.
Le traitement du MPM est à ce jour complexe et décevant avec un pronostic globalement défavorable (survie médiane <1 an), justifiant une prise en charge spécialisée dans des centres dédiés. En janvier 2012, s’est constitué un réseau clinique français de centres experts (inter) régionaux pour la prise en charge du MPM (appelé « MESOCLIN ») financé par l’Institut National contre le Cancer (INCa). Ce réseau est coordonné par le centre expert national basé au CHRU de Lille, en étroite collaboration avec le réseau MESOPATH (réseau expert national anatomo-pathologique des mésothéliomes).
L’intérêt médical pour ce cancer a évolué, passant du fatalisme à un réel investissement dans la prise en charge de cette maladie : avec la notion de chirurgie acceptable, avec de nouvelles drogues cytotoxiques et d’associations efficaces, avec l’émergence des biothérapies, avec de nouvelles modalités de radiothérapie et surtout du développement de stratégies multidisciplinaires concertées. Elles permettent actuellement de construire des essais prospectifs, comparatifs, randomisés qui faisaient largement défaut dans ce domaine. Le recrutement régional des patients porteurs d’un MPM à Lille est important. Il est lié aux nombreuses expositions professionnelles, voire environnementales ou domestiques, dans la région Hauts de France : chantiers navals, métallurgie, bâtiment…
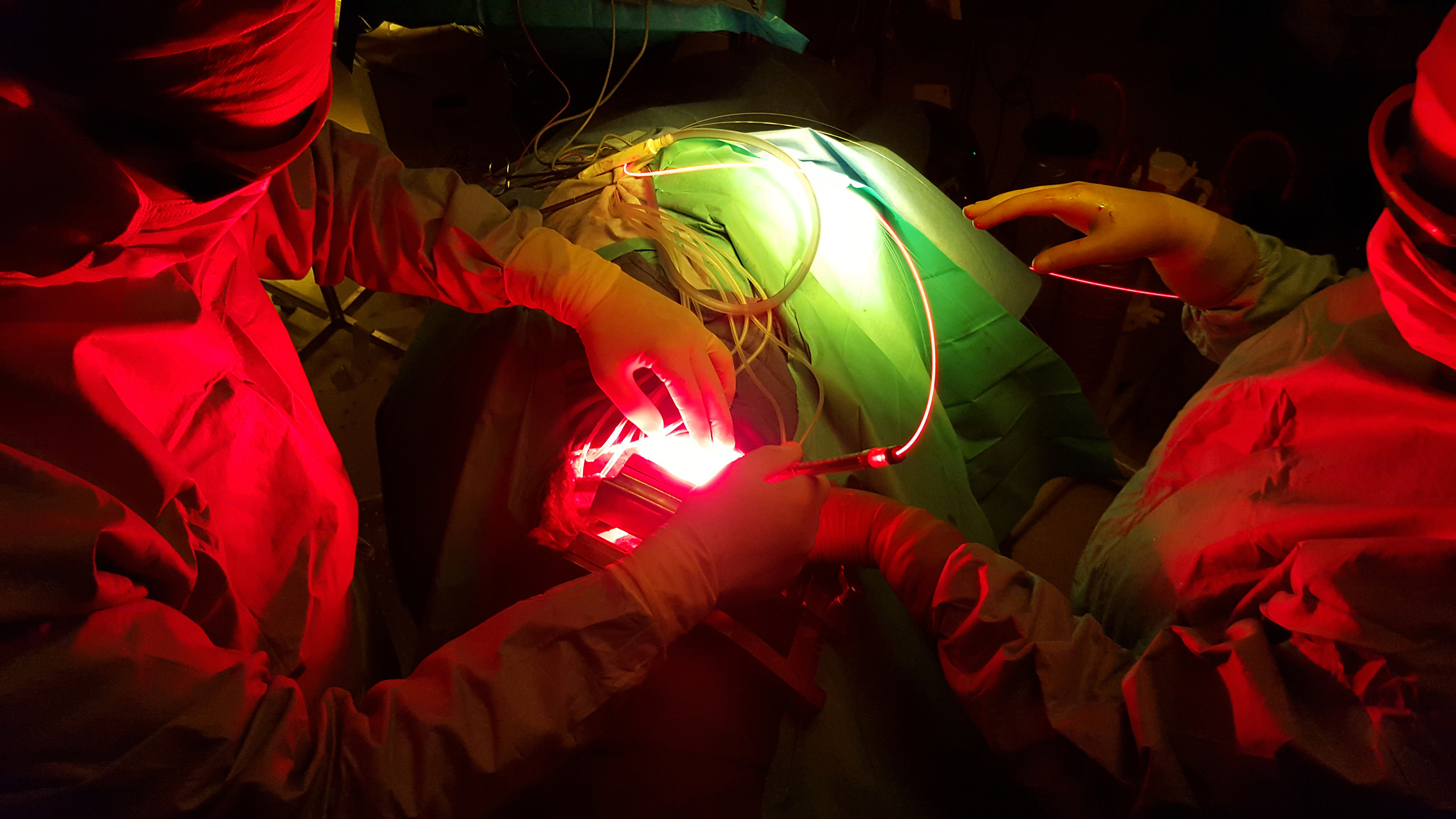
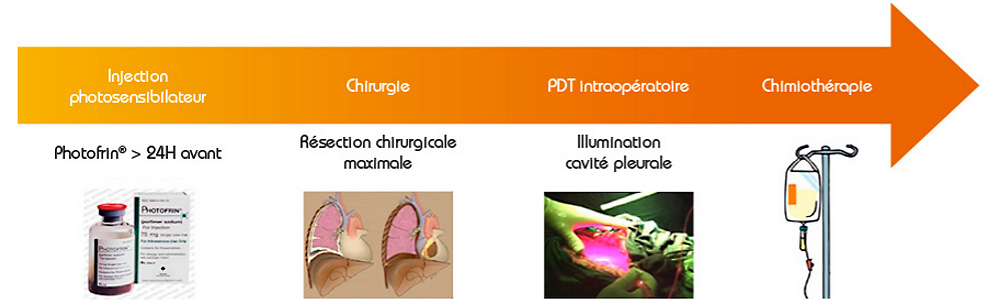
La thérapie photodynamique, ou PDT, est un traitement relativement nouveau dans le MPM. Elle se base sur le rationnel que les cellules tumorales, si elles sont d’abord traitées par un agent photosensibilisant, mourront quand elles seront exposées à une lumière émise par une source laser à une longueur d’onde spécifique. Après une résection tumorale la plus complète possible (pleurectomie et décortication, P/D), le chirurgien illumine au moyen d’un laser la cavité pleurale produisant une lumière spécifiquement absorbée par la substance photosensibilisante. Ainsi la PDT a été testée dans des essais cliniques de phase I et II pour les patients MPM en combinaison avec la PEP (pneumonectomie extra-pleurale) ou la P/D puis une chimiothérapie intraveineuse. Les premiers travaux menés par l’équipe du Professeur Friedberg (USA) ont montré des résultats prometteurs avec une survie globale médiane de 31,7 mois ([IC]95% 9-54 mois).
Objectifs
L’unité INSERM U1189, en collaboration avec le service de Pneumologie et Oncologie Thoracique et le service de Chirurgie Thoracique du CHRU de Lille, ont débuté un projet ambitieux visant à développer la PDT intrapleurale pour le MPM. Les travaux se déroulent sous deux versants : clinique et recherche.
Sur le plan clinique, l’objectif était de mettre en place la PDT intrapleurale en clinique associée à la P/D et une chimiothérapie post-opératoire, chez les patients atteints de MPM. Des contacts très avancés ont déjà eu lieu entre les deux équipes en France et aux USA, qui se connaissent de longue date. L’idée était de reproduire à l’identique les procédures chirurgicales et de PDT qui sont appliquées par l’équipe de Philadelphie, avec leur étroite collaboration.
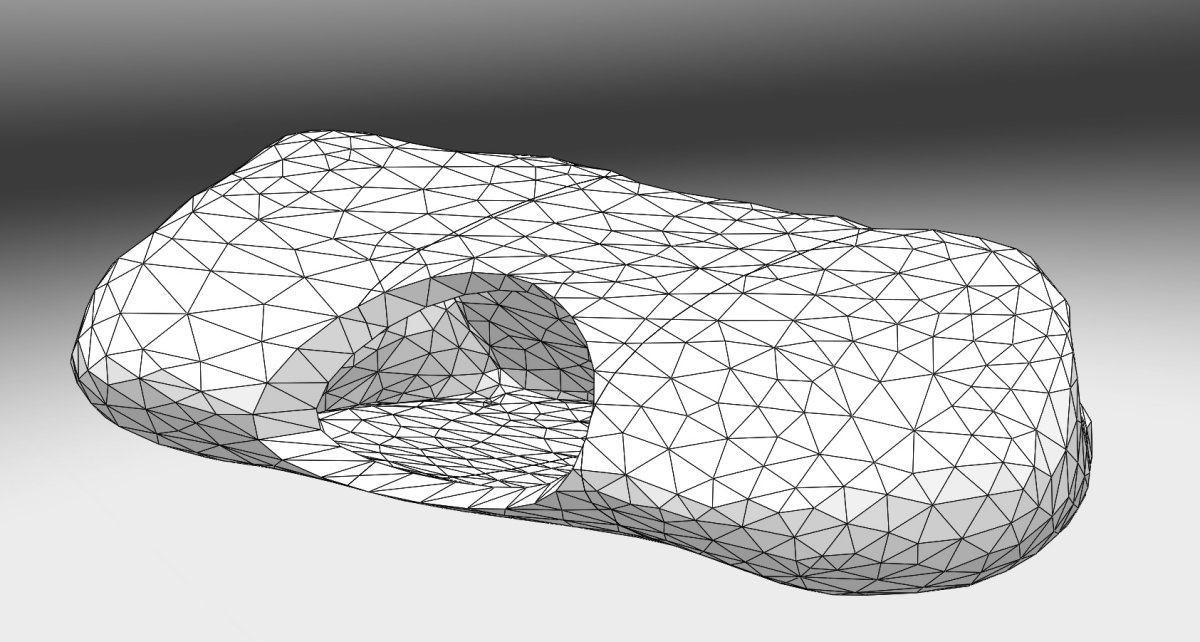
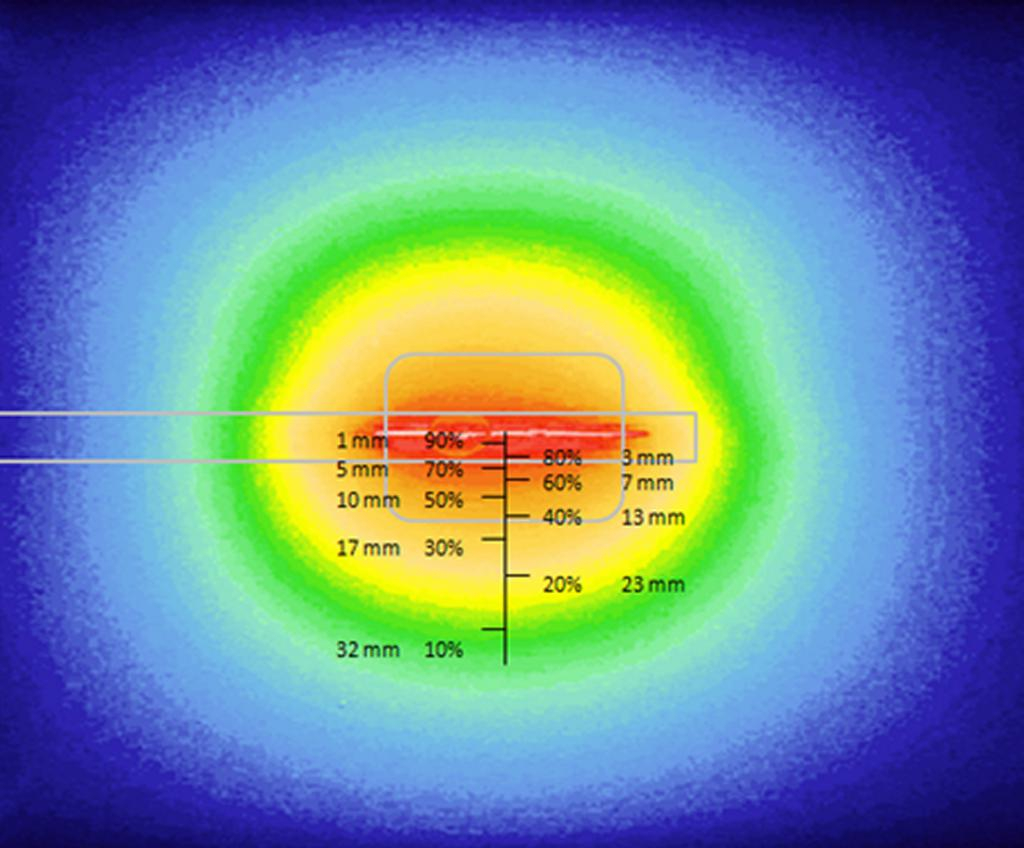
Sur le plan recherche, l’objectif était d’optimiser l’illumination par le biais du dispositif lumineux et le développement d’une méthode alternative de dosimétrie pré et per opératoire de la PDT intrapleurale. La clé de voûte de la réussite d’une procédure de PDT réside entre autres sur une illumination totale et homogène de la cavité pleurale. La technique actuelle consiste à remplir la cavité d’un liquide diffusant puis à procéder à l’illumination en « remuant » la source de lumière dans la cavité. Actuellement, la dosimétrie per opératoire est réalisée par 7 capteurs isotropes positionnés dans la cavité thoracique, mais ne renseigne pas sur la lumière délivrée entre ces points. Le programme de recherche en développement dans l’équipe INSERM U1189 se base sur les compétences, employées déjà dans pour d’autres pathologies: modélisation de l’action du laser et imagerie médicale. Le but étant d’optimiser la dosimétrie de lumière et d’assurer une application complète et homogène sur les cibles.
Où en sommes-nous ?
Grâce au soutien du Conseil Régional Hauts de France et des associations de patients, un essai local de phase II de faisabilité est actuellement en cours au CHRU de Lille. Dans le cadre d’un Programme Hospitalier de Recherche Clinique (PHRC) National Cancer retenu par l’INCa en 2013, une autre étude de phase II aura lieu ensuite. Cette fois, il s’agira d’un essai multicentrique national randomisé pour valider l’intérêt de la PDT dans le MPM.
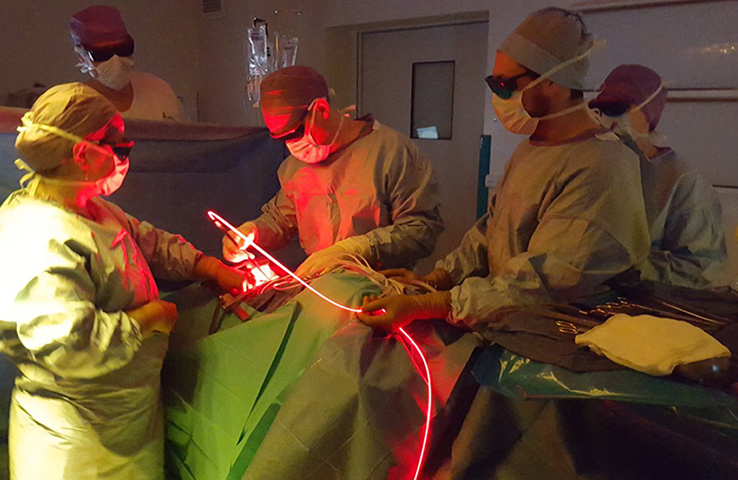
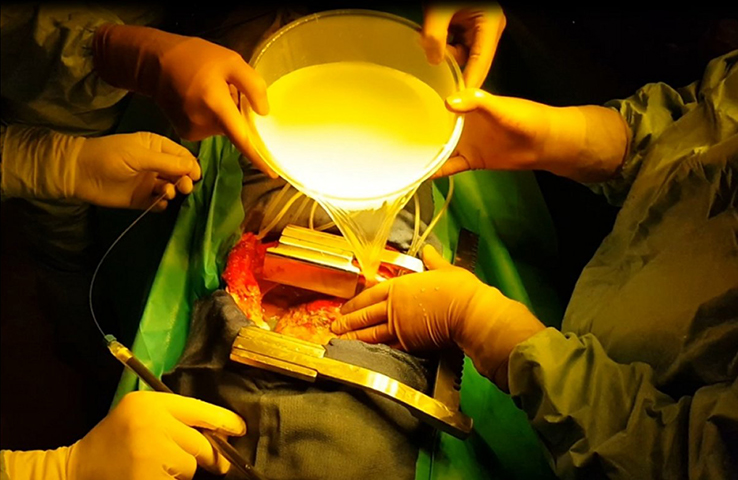
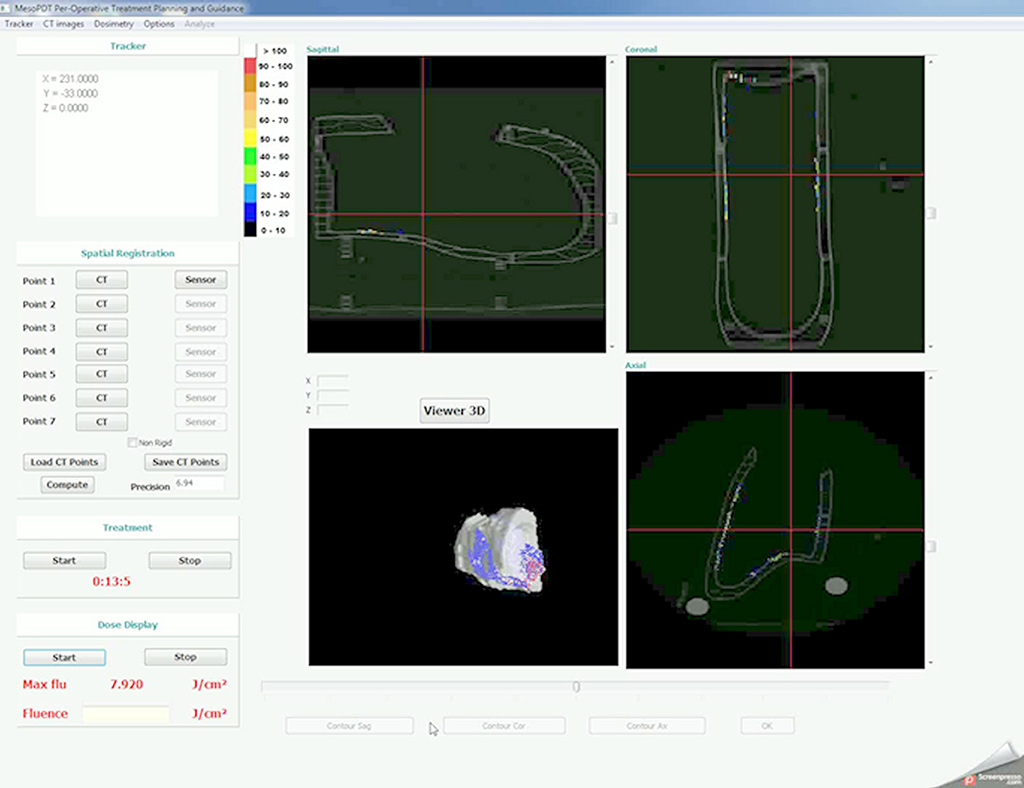
Du côté recherche, une modèle d’illumination théorique d’un dispositif lumineux a été défini et combiné à un système de repérage spatial électromagnétique, avec visualisation sur imagerie en 3D (scanner thoracique) de la dose de lumière déposée en temps réel, pour une illumination la plus complète et homogène.
Cette méthode de dosimétrie a été validée sur un fantôme de cavité thoracique intra opératoire à taille humaine, modélisé au sein du laboratoire et imprimé en 3D.
Une des autres pistes de recherche sur laquelle travaillent le laboratoire est l’utilisation de textiles lumineux. Il s’agit de dispositifs flexibles assurant l’illumination homogène d’une surface, qui pourrait donc s’appliquer à la géométrie complexe de la cavité pleurale. De récents travaux de l’Unité 1189 menés sur un modèle in-vivo de carcinose péritonéale ont montré que des illuminateurs souples permettaient d’assurer une illumination homogène.